I farmaci agonisti del recettore GLP-1 stanno ridefinendo il trattamento dell’obesità. Dalla biologia molecolare alle raccomandazioni dell’OMS, una guida completa alle terapie più promettenti degli ultimi decenni.
- Introduzione
- Cos’è l’obesità e perché è un problema globale
- Cosa sono i farmaci agonisti del recettore GLP-1
- Come funzionano i farmaci agonisti del recettore GLP-1
- Tre generazioni di farmaci a confronto: GLP-1 selettivi, Dual e Triple agonisti
- Effetti collaterali e sicurezza dei GLP-1 agonisti e degli agonisti multipli
- Le linee guida OMS: raccomandazioni e sfide globali
- Una prospettiva più ampia
- Bibliografia
Introduzione
L’obesità è una delle sfide sanitarie più urgenti del nostro tempo. Secondo l’Organizzazione Mondiale della Sanità (OMS), oltre un miliardo di persone nel mondo ne sono colpite, e i numeri continuano a crescere in quasi tutti i paesi. Non si tratta di un problema estetico o di stile di vita: l’obesità è una malattia cronica e recidivante che contribuisce a patologie come il diabete di tipo 2, le malattie cardiovascolari e alcuni tipi di cancro, e genera costi economici enormi per i sistemi sanitari di tutto il mondo.
In questo contesto, l’OMS ha pubblicato le prime linee guida sull’uso dei farmaci agonisti del recettore GLP-1 (glucagon-like peptide-1), una classe terapeutica che sta cambiando profondamente l’approccio a questa epidemia globale. Questo articolo si basa su un articolo pubblicato su JAMA il 1° dicembre 2025, che riassume quelle raccomandazioni, e si propone di illustrarne i contenuti principali: cosa sono questi farmaci, come funzionano, quali sono i benefici documentati, quali le sfide ancora aperte e cosa chiede l’OMS a governi e sistemi sanitari.
Cos’è l’obesità e perché è un problema globale
L’obesità è una malattia complessa, influenzata da fattori genetici, neurobiologici, comportamentali e ambientali. L’OMS la definisce una condizione cronica che, nella maggior parte dei casi, richiede un trattamento a lungo termine. È associata a milioni di morti premature ogni anno, in larga parte attribuibili alle malattie non trasmissibili che favorisce, e rappresenta una quota crescente della spesa sanitaria nei paesi ad alta prevalenza.
Le cause sono molteplici e si intrecciano: diete ipercaloriche, sedentarietà, diffusione globale di alimenti ultra-processati e ambienti che rendono strutturalmente difficile mantenere un peso sano.
Il quadro globale è in crescita, ma non uniforme. In alcuni paesi ad alto reddito si osservano segnali di stabilizzazione, e in alcune fasce della popolazione persino un’inversione di tendenza, probabilmente legati a politiche di salute pubblica, maggiore consapevolezza e cambiamenti nelle abitudini alimentari. Tuttavia, questi segnali positivi convivono con una crescita sostenuta nei paesi a basso e medio reddito, dove l’urbanizzazione rapida, la diffusione di alimenti ultra-processati e la riduzione dell’attività fisica stanno producendo gli stessi effetti che i paesi ricchi hanno sperimentato decenni prima. Il trend globale, nel complesso, rimane in salita.
È in questo scenario, complesso, disomogeneo e difficile da invertire con le sole politiche preventive, che l’arrivo di terapie farmacologiche efficaci assume un significato che va ben oltre la clinica.
Pubblicità
Cosa sono i farmaci agonisti del recettore GLP-1
Il GLP-1 (glucagon-like peptide-1) è un ormone prodotto dall’intestino dopo i pasti, con un compito preciso: segnalare all’organismo che il cibo è arrivato. Lo fa legandosi a una proteina presente sulla superficie di molte cellule: il recettore GLP-1. Questo legame innesca una catena di segnali che regolano la glicemia, riducono l’appetito e rallentano lo svuotamento gastrico.
I farmaci di questa classe imitano o potenziano questa azione, ma in modo prolungato. I loro effetti durano ore o giorni, invece dei pochi minuti dell’ormone naturale.
I farmaci agonisti del recettore GLP-1 sono nati inizialmente come terapia per il diabete di tipo 2: il primo fu l’exenatide (Byetta), approvato dalla FDA nel 2005 e derivato da un peptide isolato dalla saliva dell’eloderma (una lucertola nordamericana) che si era rivelato stranamente simile al GLP-1 umano pur provenendo da una specie evolutivamente distante.
Questi farmaci si sono poi rivelati efficaci anche per la perdita di peso, aprendo la strada alla loro approvazione come terapie per l’obesità. Oggi costituiscono una delle classi farmacologiche in più rapida evoluzione della medicina.
Come funzionano i farmaci agonisti del recettore GLP-1
Il meccanismo molecolare a cascata dei GLP-1 agonisti
Quando il farmaco si lega al recettore GLP-1 sulla superficie della cellula, mette in moto una reazione a catena. Il recettore attiva una proteina di segnalazione interna, la G-protein. A sua volta, la G-protein stimola un enzima, l’adenilato ciclasi, a produrre una piccola molecola chiamata cAMP.
Il cAMP è un vero e proprio “messaggero” della cellula: una volta prodotto, attiva una serie di proteine che traducono il segnale in azioni concrete.
La risposta alla cAMP si divide in due tempi., una a breve ed una seconda a lungo termine.
La via a breve termine ad effetti rapidi: la via PKA
Nel breve termine, il cAMP attiva la protein chinasi A (PKA), che agisce rapidamente su più bersagli in modo quasi simultaneo.
Nel pancreas, apre i canali del calcio nelle cellule beta e stimola il rilascio di insulina, ma solo in risposta al glucosio. Questo è un dettaglio importante: a differenza di altre terapie antidiabetiche, il rischio di ipoglicemia è significativamente ridotto. Parallelamente, frena le cellule alfa del pancreas, responsabili della produzione di glucagone, l’ormone che alza la glicemia.
A livello digestivo, rallenta lo svuotamento gastrico, prolungando il senso di pienezza dopo il pasto.
Infine, a livello cerebrale, invia segnali di sazietà all’ipotalamo e alle aree cerebrali del sistema di ricompensa, come il nucleus accumbens. In tal modo riduce sia la fame che il craving, quel desiderio intenso e difficile da ignorare per cibi dolci, salati o grassi, che va oltre la fame vera e propria.
La via a lungo termine con effetti protettivi: le cascate PI3K/AKT e MAPK
Nel lungo termine, si attivano due ulteriori cascate di segnalazione. La prima è la via PI3K/AKT; e la seconda è la via MAPK, dal nome degli enzimi coinvolti. Queste due cascate producono effetti più silenziosi ma ugualmente rilevanti.
1) La via della sopravvivenza cellulare: la via PI3K/AKT
La via PI3K/AKT protegge le cellule beta del pancreas rallentandone la morte programmata (cioè blocca l’apoptosi cellulare), favorendone così la sopravvivenza; migliora la sensibilità all’insulina nei tessuti periferici, nei muscoli e nel fegato; ed ha effetti anti-infiammatori e protettivi su cuore, reni e vasi.
PI3K sta per phosphatidylinositol 3-kinase: è un enzima che modifica una molecola grassa sulla membrana cellulare, creando un “segnale di ancoraggio” su cui si aggancia la proteina successiva, che è, appunto, l’AKT (anche chiamata col nome più corretto PKB, protein kinase B), la quale si attiva appena raggiunge la membrana e da lì fosforila (cioè “accende” o “spegne”) una serie di bersagli dentro la cellula. Il nome PI3K/AKT indica proprio questa sequenza: PI3K agisce per prima, AKT la segue.
2) La via riparativa e antinfiammatoria: la via MAPK/ERK
La via MAPK/ERK, invece, interviene nei processi di crescita e riparazione cellulare, e contribuisce anch’essa agli effetti anti-infiammatori.
MAPK sta per mitogen-activated protein kinase: è una famiglia di enzimi attivati in risposta a stimoli esterni — ormoni, fattori di crescita, stress cellulare. Nel contesto del recettore GLP-1, la variante più rilevante è ERK (extracellular signal-regulated kinase), che regola proliferazione cellulare, riparazione dei tessuti e risposta infiammatoria.
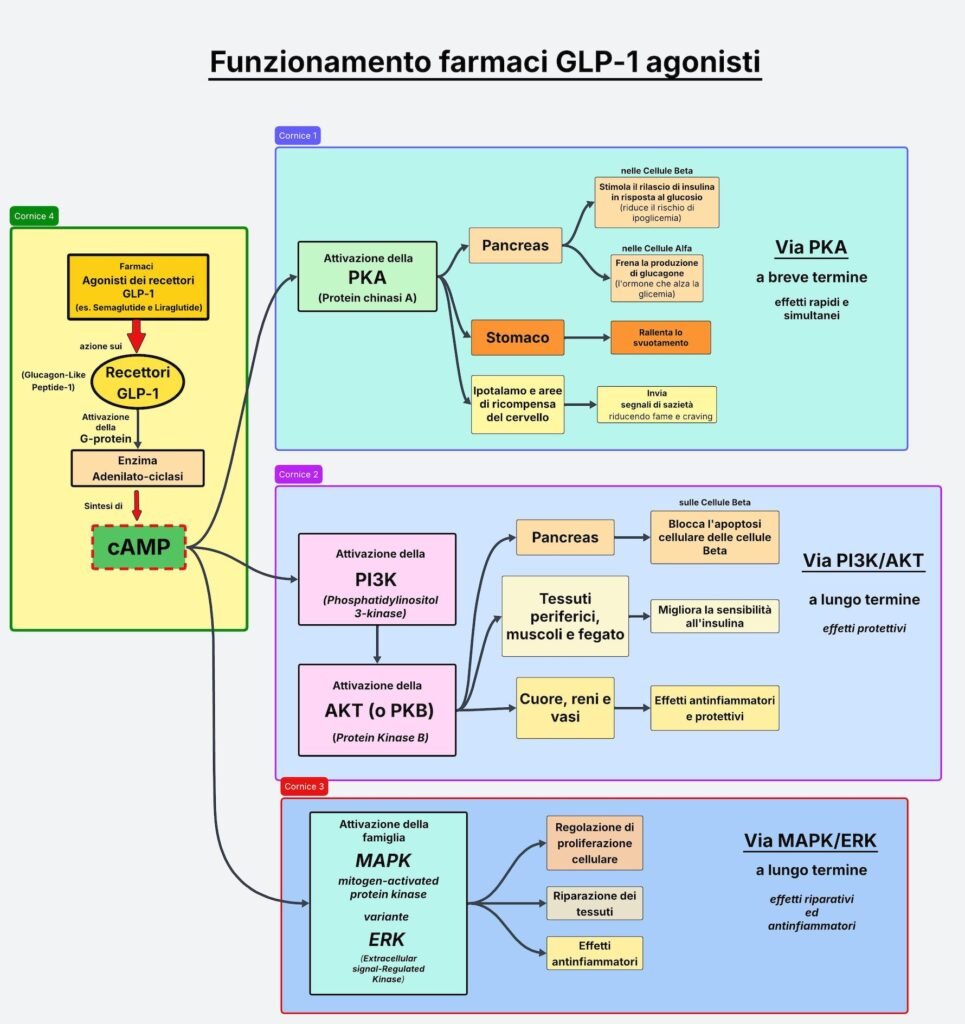
Sono questi effetti, che emergono solo dopo mesi di trattamento, a spiegare i benefici cardiovascolari e renali documentati nei grandi trial clinici, effetti che vanno ben oltre la semplice perdita di peso.
Esistono infine dati preliminari su possibili effetti neuroprotettivi, in particolare riguardo a Parkinson e Alzheimer. Si tratta tuttavia di un’area di rierca ancora aperta, non di benefici acclarati da dati scientifici solidi.
Pubblicità
Come cambia il rapporto con il cibo con gli agonisti GLP-1
A livello pratico, questi farmaci fanno dimagrire principalmente perché riducono in modo significativo la quantità di cibo assunta durante la giornata. Non bruciano calorie direttamente, ma intervengono sui meccanismi che regolano fame e sazietà.
Un meccanismo centrale
Il primo meccanismo è centrale. Il farmaco raggiunge il cervello, in particolare l’ipotalamo e le aree cerebrali legate alla ricompensa e al craving, e sopprime il segnale di fame. Il senso di sazietà arriva prima e dura più a lungo. Si riduce anche il desiderio di cibi ad alto contenuto calorico. Questo non avviene per un atto di volontà, ma perché il segnale neurobiologico che li rende attraenti viene attenuato.
La nausea, uno dei più comuni effetti collaterali di questi farmaci nelle prime settimane di trattamento, è dovuta in parte ad un effetto centrale.
Un meccanismo periferico
Il secondo meccanismo è periferico: il rallentamento dello svuotamento gastrico prolunga la sensazione fisica di pienezza dopo il pasto.
È importante notare che la nausea iniziale, che molti pazienti riferiscono nelle prime settimane di trattamento, ha però una doppia origine: in parte è legata proprio a questo rallentamento della motilità gastrica, in parte è di natura centrale, dovuta all’attivazione dei recettori GLP-1 su quelle stesse aree cerebrali (tronco encefalico e ipotalamo) che regolano la nausea e il vomito. Con la prosecuzione del trattamento, entrambi i meccanismi tendono ad attenuarsi.
Il risultato finale dei meccanismi d’azione degli GLP-1 agonisti
Il risultato combinato è una riduzione spontanea dell’introito calorico, che è il motore principale della perdita di peso. Stimata nei trial clinici nell’ordine del 20-35% rispetto al basale, questa riduzione si ottiene senza che il paziente debba seguire un piano alimentare rigido. I dati clinici mostrano che questa riduzione si mantiene nel tempo finché si assume il farmaco.
Per dare un’idea della magnitudine dell’effetto: una persona che prima consumava 2.500-3.000 calorie al giorno può scendere a 1.600-2.000 in modo naturale, semplicemente perché mangia porzioni più piccole, fa meno spuntini e ha meno craving serale. (N.B. si tratta di un esempio illustrativo, non di un dato clinico standardizzato).
Tre generazioni di farmaci a confronto: GLP-1 selettivi, Dual e Triple agonisti
I GLP-1 sono i farrmaci capostipite per il trattamento dell’obesità. La ricerca scientifica ha portato a nuove generazioni di molecole che permettono di raggiungere effetti metabolici più marcati, grazie all’azione su più tipi di recettori. Sono generazioni successive di farmaci, ognuna con un meccanismo aggiuntivo rispetto alla precedente.
GLP-1 selettivi: semaglutide e liraglutide
Gli agonisti GLP-1 selettivi, come semaglutide e liraglutide, agiscono, come visto, su un unico recettore. Il loro effetto principale è la riduzione dell’appetito, il controllo glicemico ed un rallentato svuotamento gastrico.
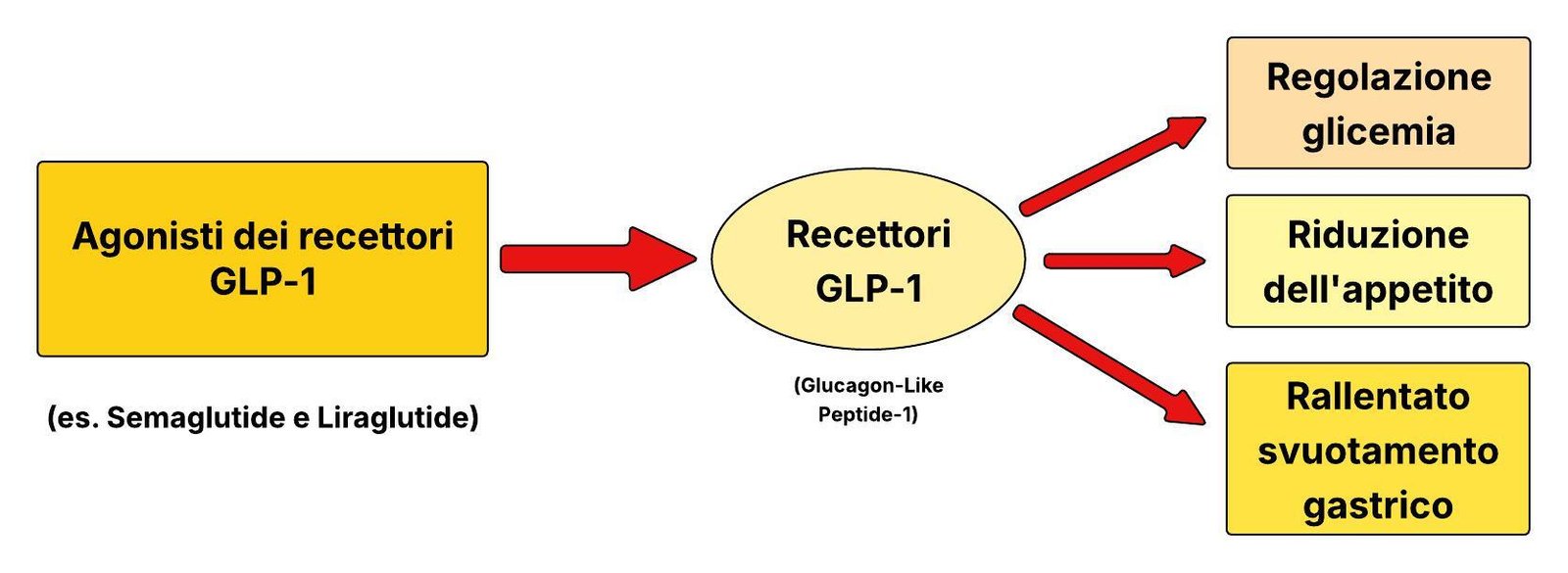
Semaglutide è l’agonista selettivo del recettore GLP-1 più diffuso. È disponibile in forma iniettiva settimanale (Wegovyper l’obesità, Ozempic per il diabete) e, dal 2025, anche in formulazione orale (Rybelsus e una versione orale di Wegovy).
Nei trial STEP ha mostrato una riduzione media del peso corporeo del 15-16% in 68 settimane con la formulazione iniettiva, e del 13-14% con quella orale.
La formulazione orale richiede assunzione a digiuno con poca acqua, il che ne limita in parte la praticità quotidiana
Liraglutide (Saxenda), approvato per l’obesità nel 2015, è stato il capostipite della classe per questa indicazione, con riduzioni di peso medie intorno al 5-8%.
Dual agonisti: tirzepatide
I dual agonisti rappresentano un salto qualitativo rispetto ai GLP-1 selettivi. Tirzepatide (Mounjaro/Zepbound) non è la combinazione di due farmaci distinti, ma un’unica molecola progettata con due porzioni funzionali distinte, ognuna complementare a due recettori diversi: quello del GLP-1 e quello del GIP (glucose-dependent insulinotropic polypeptide), un ormone prodotto anch’esso dall’intestino dopo i pasti.
Il GIP aggiunge un effetto che i GLP-1 selettivi non hanno: potenzia la risposta insulinica e, soprattutto, stimola la lipolisi nel tessuto adiposo, cioè la scissione dei trigliceridi immagazzinati nelle cellule grasse.
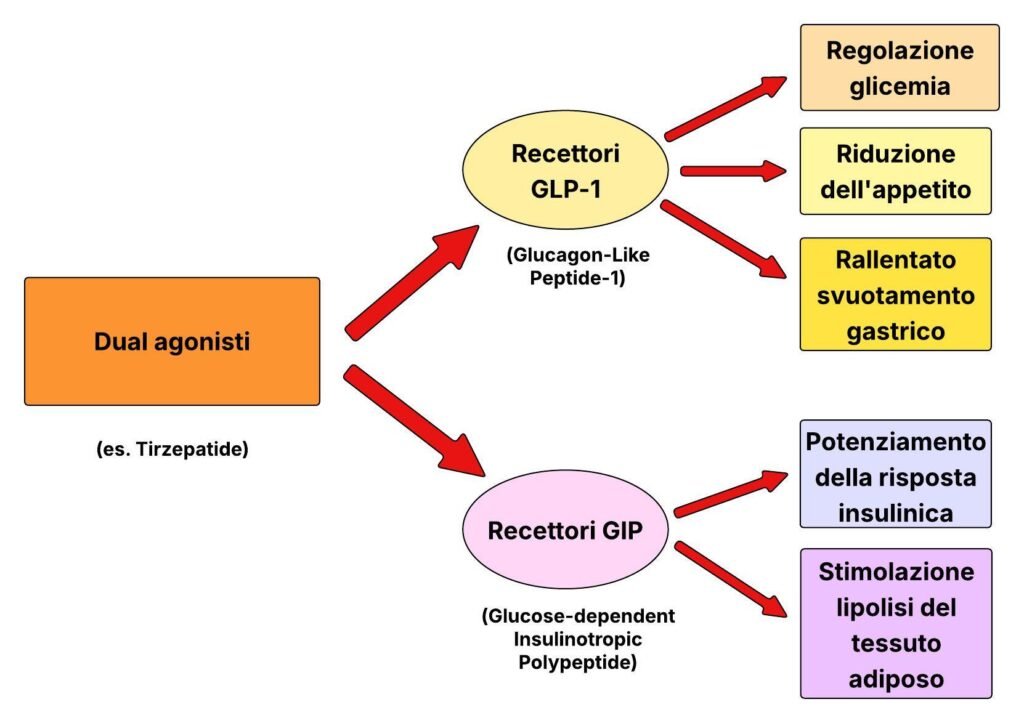
In pratica, tirzepatide non solo riduce quanto si mangia, ma in più spinge l’organismo a utilizzare più attivamente le riserve di grasso. Questo spiega, almeno in parte, perché la perdita di peso media nei trial sia significativamente superiore a quella dei GLP-1 selettivi. Nei trial SURMOUNT la riduzione media del peso ha raggiunto il 20-22% in 72 settimane.
Triple agonisti
I triple agonisti, come retatrutide (ancora in fase di sperimentazione), possiedono una struttura molecolare con tre porzioni funzionali distinte, ognuna progettata per legarsi ad un recettore specifico. Ai recettori GLP-1 e GIP, si aggiunge quindi un terzo bersaglio: il recettore del glucagone.
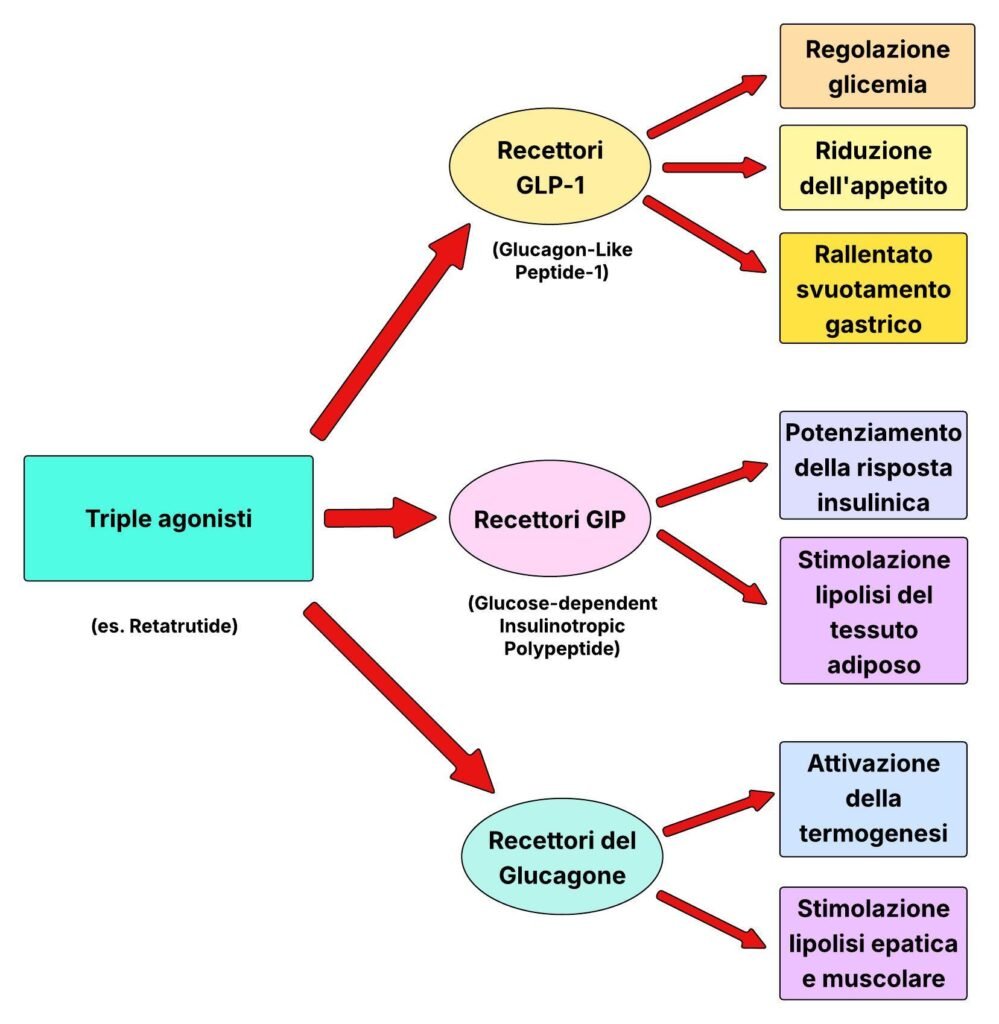
Il glucagone è un ormone prodotto dal pancreas con una funzione primaria opposta all’insulina (alza la glicemia liberando glucosio dal fegato). Tuttavia, nei triple agonisti il glucagone viene attivato in modo controllato e mirato, sfruttando un suo effetto secondario: aumentare la spesa energetica a riposo attraverso la termogenesi, cioè la produzione di calore da parte dell’organismo, e stimolare la lipolisi a livello epatico e muscolare.
Il risultato è che il corpo brucia più energia anche a riposo, oltre a mangiare meno e a utilizzare meglio i grassi. Si tratta di tre leve che agiscono contemporaneamente, il che spiega le riduzioni di peso più marcate osservate con questa classe. Nei dati preliminari, infatti, le riduzioni di peso osservate sono state le più marcate finora, nell’ordine del 24-29%, avvicinandosi per la prima volta agli effetti prodotti dalla chirurgia bariatrica con un approccio farmacologico.
Questi effetti metabolici aggiuntivi non sono il motore principale della perdita di peso, che resta in tutti i casi la riduzione spontanea dell’introito calorico. Tuttavia contribuiscono in modo rilevante a spiegare perché l’efficacia aumenta progressivamente passando da una generazione all’altra.
Retatrutide è un agonista triplice (GLP-1, GIP e recettore del glucagone) ancora in fase 3 di sperimentazione, con un’approvazione FDA attesa tra il 2026 e il 2027.
Un altro candidato di interesse è UBT251, sviluppato inizialmente in Cina e ora oggetto di un accordo globale con Novo Nordisk. Ha mostrato risultati promettenti in fase II, ma i dati sono ancora preliminari e i confronti con tirzepatide sono indiretti: andranno confermati in trial comparativi diretti.
Una novità di natura diversa: orforglipron
Orforglipron rappresenta un’innovazione di tipo diverso rispetto ai precedenti: è il primo farmaco, tra quelli che si possono assumere per via orale, che non è un peptide: cioè è di sintesi e non deriva da una proteina. Sviluppata da Eli Lilly, si attende una decisione della FDA nel 2026.
A differenza dei farmaci peptidici orali come Rybelsus (semaglutide), non richiede restrizioni alimentari per l’assunzione, il che potrebbe migliorarne significativamente l’aderenza nella pratica quotidiana. Nei trial ha mostrato riduzioni di peso dell’11-12% e risultati superiori al semaglutide orale nel controllo glicemico.
Pubblicità
Effetti collaterali e sicurezza dei GLP-1 agonisti e degli agonisti multipli
Gli effetti collaterali gastrointestinali: i più comuni, ma gestibili
Il profilo di tollerabilità di questi farmaci è nel complesso ben documentato, con dati che oggi coprono milioni di pazienti-anno. Gli effetti indesiderati più comuni riguardano l’apparato gastrointestinale e si concentrano nelle prime settimane di trattamento, durante la fase di titolazione, il periodo in cui la dose viene aumentata gradualmente per migliorare la tollerabilità.
Nausea, vomito, diarrea e stipsi sono i disturbi più frequenti, con incidenze che nei trial clinici variano indicativamente tra il 30 e il 55% per la nausea e tra il 10 e il 25% per il vomito. Questi effetti tendono ad attenuarsi con il tempo e sono in parte gestibili rallentando ulteriormente la titolazione o, nelle fasi iniziali, con l’uso temporaneo di antiemetici.
La frequenza aumenta con la complessità del meccanismo d’azione: i triple agonisti come retatrutide mostrano effetti gastrointestinali più marcati rispetto ai dual come tirzepatide, che a sua volta li mostra più frequentemente rispetto ai GLP-1 selettivi come semaglutide. Orforglipron si colloca su livelli simili o leggermente superiori a semaglutide orale.
Altri effetti comuni: cefalea, affaticamento e ipoglicemia
Tra gli altri effetti comuni si segnalano cefalea, affaticamento e una lieve tachicardia, quest’ultima più associata ai farmaci che includono l’azione sul glucagone.
L’ipoglicemia, cioè l’abbassamento eccessivo della glicemia, è rara e si manifesta quasi esclusivamente nei pazienti che assumono contemporaneamente insulina o sulfoniluree, una classe di farmaci antidiabetici che stimola direttamente il rilascio di insulina.
Effetti gravi: rari e sotto controllo
Gli effetti gravi sono poco frequenti.
La pancreatite è stata oggetto di attenzione fin dalle prime approvazioni, ma i dati dei trial mostrano un’incidenza sovrapponibile a quella del placebo.
La colelitiasi, cioè la formazione di calcoli biliari, è un rischio reale, legato in parte alla rapida perdita di peso piuttosto che al farmaco in sé. La rapida perdita di peso porta a un aumento della secrezione di colesterolo nella bile e a una riduzione dello svuotamento della colecisti, creando le condizioni per la formazione dei calcoli. Quindi è un effetto indiretto della terapia, non una tossicità diretta del farmaco, ma comunque un rischio da conoscere e monitorare.
Sul fronte dei tumori tiroidei, l’allerta emersa negli studi su roditori non si è tradotta, finora, in un segnale clinico rilevante nell’uomo.
Le aree ancora sotto osservazione
Due aspetti restano oggetto di monitoraggio attivo.
Il primo riguarda la composizione corporea: una perdita di peso rapida e marcata può accompagnarsi a una riduzione della massa muscolare, e il monitoraggio della sarcopenia, cioè la perdita progressiva di massa e forza muscolare, è considerato parte integrante del follow-up clinico.
Il secondo riguarda possibili effetti su dipendenze e funzioni cognitive, segnalati in studi preliminari ma ancora privi di dati sufficienti per trarre conclusioni definitive.
Quanto è frequente l’interruzione del trattamento?
Il tasso di interruzione per effetti collaterali si attesta, a seconda degli studi, tra il 10 e il 20%: una quota non trascurabile, che sottolinea l’importanza di una titolazione attenta e di un supporto clinico continuativo, soprattutto nelle prime settimane.
Pubblicità
Le linee guida OMS: raccomandazioni e sfide globali
Nel 2024 l’OMS ha pubblicato le prime linee guida dedicate all’uso dei farmaci agonisti del recettore GLP-1 nel trattamento dell’obesità negli adulti. Si tratta di un documento elaborato con il metodo GRADE (uno standard internazionale per la valutazione delle evidenze) e costruito con il contributo di esperti clinici, rappresentanti dei pazienti e professionisti della sanità pubblica di diversi paesi.
L’obiettivo non è solo clinico: le linee guida nascono dalla consapevolezza che questi farmaci esistono, funzionano, ma rischiano di essere accessibili solo a una minoranza della popolazione mondiale che ne avrebbe bisogno.
Cosa raccomanda l’OMS
Le raccomandazioni si articolano su due livelli.
Le dichiarazioni di buona pratica: l’obesità come malattia cronica
Il primo è quello delle dichiarazioni di buona pratica, che non richiedono prove dirette perché riflettono principi clinici consolidati: l’obesità va trattata come malattia cronica, con screening, diagnosi precoce e gestione continuativa delle comorbidità; e a tutti i pazienti vanno offerti, come punto di partenza, consigli su alimentazione e attività fisica, indipendentemente dal percorso terapeutico successivo.
Le due raccomandazioni “condizionali
Il secondo livello comprende due raccomandazioni cosiddette “condizionali”. Nel sistema GRADE, questa classificazione non esprime un dubbio sull’efficacia, ma indica che i benefici superano i rischi con un’incertezza residua sufficiente da richiedere una valutazione individualizzata, tenendo conto del contesto del paziente e del sistema sanitario.
1) Durata del trattamento
La prima raccomanda l’uso dei GLP-1 per almeno sei mesi come trattamento cronico negli adulti con obesità, sulla base di evidenze di qualità moderata su perdita di peso e miglioramenti metabolici. Questa soglia temporale non rappresenta una durata target, ma il minimo necessario per una prima valutazione dell’efficacia: l’indicazione reale è per un trattamento a lungo termine, potenzialmente indefinito.
È una scelta coerente con la natura della malattia. L’obesità è una condizione cronica, non un episodio acuto che si risolve con un ciclo di terapia: richiede una gestione continuativa, con la stessa logica con cui si tratta l’ipertensione o il diabete di tipo 2. I dati sulla sospensione del trattamento lo confermano chiaramente: nella maggior parte dei casi, interrompere il farmaco è seguito da un recupero sostanziale del peso perso. In altre parole, questi farmaci non guariscono l’obesità, ma la gestiscono, finché vengono assunti.
2) La terapia comportamentale intensiva
La seconda raccomanda di associare il trattamento farmacologico a una terapia comportamentale intensiva, che include obiettivi strutturati per esercizio fisico, alimentazione e counseling regolare, anche se qui la qualità delle evidenze è classificata come bassa e la variabilità tra pazienti è significativa.
L’OMS ha inoltre incluso i GLP-1 nella sua Lista dei Medicinali Essenziali, ma in modo selettivo: per ora solo per i sottogruppi ad alto rischio, ovvero pazienti con obesità associata a diabete di tipo 2, malattie cardiovascolari o malattia renale cronica.
Le sfide: accesso, equità e sistemi sanitari
La pubblicazione delle linee guida apre una questione che va ben oltre la clinica. Si stima che la capacità produttiva attuale di questi farmaci copra una frazione molto piccola delle persone che ne avrebbero indicazione a livello globale, meno del 10% secondo alcune stime, con tutti i margini di incertezza che una cifra del genere comporta. I costi restano elevati e inaccessibili per la maggior parte dei sistemi sanitari a basso e medio reddito.
L’OMS individua alcune soluzioni possibili: lo sviluppo di versioni generiche man mano che le protezioni brevettuali sulle singole molecole vengono meno nei diversi paesi, l’implementazione di prezzi differenziati per contesto economico, e il rafforzamento delle capacità produttive locali attraverso licenze volontarie e partnership pubblico-private. È un percorso lungo, e l’inclusione nella Lista dei Medicinali Essenziali è un primo passo simbolico e pratico in questa direzione.
C’è poi una sfida strutturale che riguarda i sistemi sanitari anche nei paesi ad alto reddito: integrare un trattamento cronico, che richiede titolazione progressiva, monitoraggio regolare e supporto comportamentale, nelle cure primarie non è banale. Richiede formazione, risorse e un’organizzazione che in molti contesti non esiste ancora.
Una prospettiva più ampia
Le linee guida OMS rappresentano un cambiamento di paradigma nel modo in cui la medicina istituzionale inquadra l’obesità: non più una condizione legata allo stile di vita individuale, ma una malattia cronica che richiede trattamento medico continuativo, con un approccio privo di pregiudizi e con gli stessi criteri con cui si gestisce l’ipertensione o il diabete. È un riconoscimento importante, anche culturalmente.
I farmaci GLP-1 e i loro successori multi-recettoriali sono lo strumento farmacologico più efficace mai disponibile contro l’obesità. Ma i farmaci da soli non bastano. Su questo l’OMS è esplicita : affrontare l’epidemia richiede parallelamente politiche alimentari, ambienti urbani che favoriscano l’attività fisica, contrasto alla povertà come determinante strutturale dell’obesità, e sistemi sanitari capaci di offrire un’assistenza integrata. Usare bene questi farmaci, e renderli accessibili a chi ne ha più bisogno, è una sfida che appartiene alla politica sanitaria tanto quanto alla medicina.
Le informazioni contenute in questo articolo sono a scopo informativo e non costituiscono una raccomandazione terapeutica. Le informazioni sui farmaci in fase di sperimentazione riflettono i dati disponibili al momento della pubblicazione e alcuni dati potrebbero aggiornarsi. Alcuni farmaci citati non sono ancora approvati dalle autorità regolatorie. Parla sempre con il tuo medico prima di prendere qualsiasi decisione sulla tua salute.
Pubblicità
Bibliografia
1. Linee guida OMS sull’uso dei GLP-1 per l’obesità
Celletti F, Farrar J, De Regil L. World Health Organization Guideline on the Use and Indications of Glucagon-Like Peptide-1 Therapies for the Treatment of Obesity in Adults. JAMA. 2026;335(5):434-438. doi:10.1001/jama.2025.24288 Link diretto (JAMA Network – full text gratuito con guest access): https://jamanetwork.com/journals/jama/fullarticle/2842199
Link PubMed: https://pubmed.ncbi.nlm.nih.gov/41324410/
2. Meccanismi di azione dei GLP-1 (e multi-agonisti)
Liu QK, et al. Mechanisms of action and therapeutic applications of GLP-1 and dual GIP/GLP-1 receptor agonists. Front Endocrinol (Lausanne). 2024;15:1417287. doi:10.3389/fendo.2024.1417287 Link full text (open access): https://www.frontiersin.org/journals/endocrinology/articles/10.3389/fendo.2024.1417287/full PubMed: https://pubmed.ncbi.nlm.nih.gov/39114288/
Drucker DJ. Mechanisms of Action and Therapeutic Application of Glucagon-like Peptide-1. Cell Metab. 2018;27(4):740-756. doi:10.1016/j.cmet.2018.03.001 Link (abstract gratuito; full text a pagamento o istituzionale): https://www.cell.com/cell-metabolism/fulltext/S1550-4131(18)30154-3 PubMed: https://pubmed.ncbi.nlm.nih.gov/29617641/
Moiz A, et al. Mechanisms of GLP-1 Receptor Agonist-Induced Weight Loss: A Review of Central and Peripheral Pathways in Appetite and Energy Regulation. Curr Obes Rep. 2025. doi:10.1007/s13679-025-00612-4 Link (abstract gratuito; full text a pagamento): https://link.springer.com/article/10.1007/s13679-025-00612-4 PubMed: https://pubmed.ncbi.nlm.nih.gov/39892489/
3. Efficacia clinica e perdita di peso
Jastreboff AM, et al. Triple-Hormone-Receptor Agonist Retatrutide for Obesity – A Phase 2 Trial. N Engl J Med. 2023;389(6):514-526. doi:10.1056/NEJMoa2301972 Link full text (open access): https://www.nejm.org/doi/full/10.1056/NEJMoa2301972 PubMed: https://pubmed.ncbi.nlm.nih.gov/37366315/
Garvey WT, et al. Tirzepatide once weekly for the treatment of obesity in people with type 2 diabetes (SURMOUNT-2): a double-blind, randomised, multicentre, placebo-controlled, phase 3 trial. Lancet. 2023;402(10402):613-626. doi:10.1016/S0140-6736(23)01200-X Link (abstract gratuito; full text a pagamento): https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(23)01200-X/fulltext PubMed: https://pubmed.ncbi.nlm.nih.gov/37385275/
Wharton S, et al. Once-weekly semaglutide 7·2 mg in adults with obesity (STEP UP): a randomised, controlled, phase 3b trial. Lancet Diabetes Endocrinol. 2025;13(11):949-963. doi:10.1016/S2213-8587(25)00226-8 Link (abstract gratuito; full text a pagamento): https://www.thelancet.com/journals/landia/article/PIIS2213-8587(25)00226-8/fulltext PubMed: https://pubmed.ncbi.nlm.nih.gov/40961952/
4. Effetti collaterali e sicurezza
Moiz A, et al. Efficacy and Safety of Glucagon-Like Peptide-1 Receptor Agonists for Weight Loss Among Adults Without Diabetes: A Systematic Review of Randomized Controlled Trials. Ann Intern Med. 2025. doi:10.7326/ANNALS-24-01234 Link (abstract gratuito; full text open access in molti casi): https://www.acpjournals.org/doi/10.7326/ANNALS-24-01234 PubMed: https://pubmed.ncbi.nlm.nih.gov/39761578/
Jalleh RJ, et al. The science of safety: adverse effects of GLP-1 receptor agonists as glucose-lowering and obesity medications. J Clin Invest. 2026;136(3):e194740. doi:10.1172/JCI194740 Link full text (open access): https://www.jci.org/articles/view/194740 PubMed: https://pubmed.ncbi.nlm.nih.gov/41697736/
Kunutsor SK, et al. Safety and Tolerability of Glucagon-Like Peptide-1 Receptor Agonists: A State-of-the-Art Narrative Review. Drugs. 2025. doi:10.1007/s40265-025-02145-7 Link (abstract gratuito; full text a pagamento): https://link.springer.com/article/10.1007/s40265-025-02145-7 PubMed: https://pubmed.ncbi.nlm.nih.gov/41351656/
5. Triple agonisti (focus su retatrutide)
Jastreboff AM, et al. Triple-Hormone-Receptor Agonist Retatrutide for Obesity – A Phase 2 Trial. N Engl J Med. 2023;389(6):514-526. doi:10.1056/NEJMoa2301972 Link full text (open access): https://www.nejm.org/doi/full/10.1056/NEJMoa2301972 PubMed: https://pubmed.ncbi.nlm.nih.gov/37366315/
Goldney J, et al. Triple Agonism Based Therapies for Obesity. Curr Opin Endocrinol Diabetes Obes. 2025. doi:10.1097/MED.0000000000000894 Link (abstract gratuito; full text a pagamento): https://journals.lww.com/co-endocrinology/abstract/9900/triple_agonism_based_therapies_for_obesity.123.aspx PubMed: https://pubmed.ncbi.nlm.nih.gov/40741227/
Sanyal AJ, et al. Triple hormone receptor agonist retatrutide for metabolic dysfunction-associated steatotic liver disease: a randomized phase 2a trial. Nat Med. 2024;30(7):2037-2048. doi:10.1038/s41591-024-03018-2 Link (abstract gratuito; full text open access in molti casi): https://www.nature.com/articles/s41591-024-03018-2 PubMed: https://pubmed.ncbi.nlm.nih.gov/38858523/
Tewari J, et al. Efficacy and safety of triple hormone receptor agonist retatrutide for the management of obesity: a systematic review and meta-analysis. Expert Rev Clin Pharmacol. 2025;18(1-2):51-66. doi:10.1080/17512433.2025.2450254 Link (abstract gratuito; full text a pagamento): https://www.tandfonline.com/doi/full/10.1080/17512433.2025.2450254 PubMed: https://pubmed.ncbi.nlm.nih.gov/39817343/
Pubblicità
Pubblicità



wish you best and best
Tanks 👍