Sapevi che nel tuo intestino vive un ecosistema complesso quanto una foresta pluviale? È il microbioma intestinale: 38 trilioni di batteri che non sono semplici ospiti, ma un vero e proprio “secondo cervello” capace di influenzare ogni aspetto della tua salute. Infatti, il microbioma intestinale non è solo coinvolto nella digestione, ma regola il sistema immunitario, produce neurotrasmettitori che modulano l’umore, influenza il metabolismo e può persino determinare la tua longevità. Questa guida ti condurrà attraverso le scoperte più recenti pubblicate su riviste scientifiche internazionali, svelando come la diversità microbica sia direttamente collegata alla prevenzione di malattie croniche, disturbi mentali e invecchiamento accelerato. In particolare, scoprirai strategie concrete per ottimizzare il tuo microbioma attraverso alimentazione mirata, prebiotici, probiotici e modifiche dello stile di vita, per trasformare così in maniera radicale il tuo benessere fisico e mentale.
_
- Introduzione: il microbioma intestinale
- Cos’è il microbioma intestinale?
- Le funzioni principali del microbioma: molto più della digestione
- Cosa influenza il microbioma intestinale e come prendersene cura
- Alimentazione: il fattore più potente per modellare il microbioma
- Prebiotici: il “cibo” che nutre i tuoi batteri buoni
- Probiotici: i i batteri benefici che introduci con l’alimentazione
- Combinare prebiotici e probiotici: il segreto dell’approccio sinbiotico
- Polifenoli: efficaci per la diversità del microbioma intestinale
- L’importanza della diversificazione vegetale
- Alimenti e abitudini da limitare per proteggere il microbioma
- Stile di vita
- Prospettive future e frontiere della ricerca
- Conclusione: investi nel tuo microbioma, investi nella tua salute
- Riferimenti Scientifici
- 1. Definizione, composizione e ruolo generale del microbioma nella salute umana
- 2. Sviluppo precoce del microbioma (early-life)
- 3. Interazione con il sistema immunitario
- 4. Metaboliti (SCFAs) e loro effetti sulla salute
- 5. Asse intestino-cervello (gut-brain axis)
- 6. Influenza dello stile di vita sul microbioma
- 7. Interventi pratici (probiotici, prebiotici, sinbiotici, postbiotici)
- 8. Postbiotici e psychobiotics
Introduzione: il microbioma intestinale
Nell’intestino di ognuno di noi vive un complesso ecosistema formato da circa 38 trilioni di microrganismi (un numero paragonabile alle cellule del corpo): è il microbioma intestinale, e, come vedremo, può essere considerato un vero e proprio secondo cervello.
Questi microrganismi non sono semplici ospiti passivi: al contrario, formano un vero e proprio organo metabolico che influenza profondamente digestione, sistema immunitario, umore, metabolismo e persino la longevità. Le ricerche scientifiche più recenti hanno iinfatti definito il microbioma come un “organo connettore” tra nutrizione e salute globale, capace di modulare l’assorbimento dei nutrienti e la risposta infiammatoria dell’organismo. In altre parole, questa definizione evidenzia come il microbioma non sia semplicemente un insieme di batteri, ma un vero ecosistema funzionale che dialoga costantemente con tutti i sistemi del nostro corpo.
Inoltre, gli studi più recenti hanno rivelato che il microbioma intestinale possiede un genoma collettivo – il microbioma vero e proprio – che supera di oltre 100 volte il genoma umano in termini di geni funzionali.
Questa enorme capacità genetica conferisce di conseguenza al microbioma abilità metaboliche che il nostro organismo da solo non potrebbe mai possedere: dalla sintesi di vitamine essenziali come la vitamina K e alcune vitamine del gruppo B, alla produzione di neurotrasmettitori che influenzano direttamente il nostro stato d’animo.
E quindi perché recentemente la discussione riguardo il microbioma intestinale è diventata un tema così rilevante? Grazie ai progressi nel sequenziamento del DNA e agli studi longitudinali, sappiamo ora che una composizione microbica diversificata è associata a minor rischio di malattie croniche, mentre la disbiosi (squilibrio microbico) è collegata a obesità, disturbi mentali, malattie autoimmuni e invecchiamento accelerato.
Pubblicità
Cos’è il microbioma intestinale?
Per comprendere appieno il ruolo di questo “ecosistema invisibile”, partiamo dalle definizioni precise.
Il microbiota intestinale
Il termine microbiota intestinale si riferisce all’insieme dei microrganismi vivi, principalmente batteri, ma anche virus, funghi, archea e protozoi, che colonizzano il tratto gastrointestinale, con la maggiore concentrazione nel colon.
Il microbioma intestinale
Il microbioma, invece, è il corredo genetico completo di questi microrganismi: l’insieme dei loro geni, che supera di gran lunga il numero di geni del genoma umano (circa 23.000 geni umani contro milioni nel microbioma).
In altre parole: il microbiota è la popolazione vivente, mentre il microbioma rappresenta il loro “potenziale funzionale”, ovvero ciò che questi microrganismi sono in grado di fare: dalla produzione di vitamine essenziali alla modulazione del sistema immunitario, dalla sintesi di neurotrasmettitori alla protezione contro patogeni.
Nota terminologica
Dal 2007-2008 (con l’inizio del Human Microbiome Project) il termine microbioma è diventato dominante nella letteratura anglo-americana perché mette l’accento sul potenziale funzionale (cioè su cosa quei microrganismi possono fare per noi), che è ciò che interessa di più in termini di salute. Anche nella letteratura scientifica italiana si usa spesso “microbioma intestinale” usato in senso lato.
In questo articolo (ed in quelli che verranno) useremo prevalentemente il termine microbioma intestinale come ormai consolidato nella letteratura scientifica e divulgativa, anche quando ci riferiamo alla popolazione microbica vera e propria (microbiota). La distinzione rigorosa tra i due termini esiste, ma per semplicità e continuità con la maggior parte delle fonti recenti adotteremo “microbioma” in senso ampio.
Composizione: i batteri principali
In un adulto sano vivono tra 500 e 1.000 specie batteriche diverse, con una composizione dominata da quattro phyla principali (King et al, 2019):
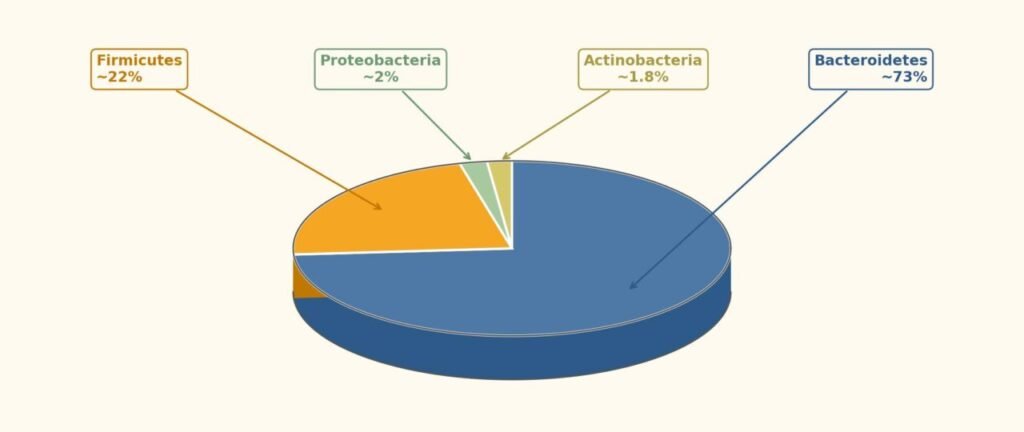
- Bacteroidetes ~73% (come Bacteroides e Prevotella),
- Firmicutes ~22% (tra cui generi come Lactobacillus e Clostridium),
- Proteobacteria ~2% (inclusi Escherichia e altri).
- Actinobacteria ~1.8% (ad esempio Bifidobacterium),
Bacteroidetes e Firmicutes rappresentano insieme oltre il 90% della composizione totale, anche se loro rapporto varia significativamente tra individui e popolazioni.
Tuttavia, la diversità è l’indicatore chiave di salute: un microbiota ricco e vario è più resiliente e meglio attrezzato per affrontare stress, patogeni e cambiamenti.
Al contrario, una bassa diversità microbica, tipica degli stili di vita occidentali caratterizzati da dieta povera di fibre, è costantemente associata a disbiosi e aumento del rischio di malattie croniche.
Studi recenti hanno dimostrato che la diversità microbica non è solo una questione di numero di specie, ma anche di equilibrio funzionale: un microbioma sano mantiene un delicato equilibrio tra batteri produttori di metaboliti benefici e quelli potenzialmente pro-infiammatori. In questo senso, la definizione stessa di “microbioma sano” considera non solo la composizione batterica, ma anche la funzionalità metabolica e la capacità di resilienza dell’ecosistema intestinale.
Pubblicità
Le funzioni principali del microbioma: molto più della digestione
Il microbioma intestinale svolge funzioni vitali che vanno ben oltre la semplice digestione degli alimenti. Agisce come un vero e proprio organo metabolico e immunomodulatore.
Produzione di metaboliti essenziali: gli acidi grassi a catena corta (SCFAs)
I batteri intestinali fermentano le fibre alimentari producendo acidi grassi a catena corta (SCFAs), principalmente acetato, propionato e butirrato.
Tra questi, il butirrato è particolarmente importante: rappresenta la fonte energetica primaria per i colonociti (le cellule del colon) fornendo fino al 10% del fabbisogno calorico giornaliero totale.
Tuttavia, le funzioni degli SCFAs vanno ben oltre l’energia: acetato e propionato vengono assorbiti e trasportati al fegato dove influenzano la gluconeogenesi e la sintesi di colesterolo, mentre il butirrato esercita potenti effetti anti-infiammatori (attraverso l’inibizione dell’istone deacetilasi), riducendo l’infiammazione sistemica di basso grado.
Inoltre, studi recenti hanno dimostrato che gli SCFAs influenzano anche il metabolismo di glucosio e lipidi contribuendo al controllo glicemico e alla sensibilità insulinica, oltre ad avere effetti benefici sulla salute cardiovascolare modulando la pressione sanguigna attraverso recettori specifici (GPR41 e GPR43) presenti nelle cellule vascolari e renali.
Sistema immunitario: l’educazione microbica
Il 70-80% delle cellule immunitarie risiede nell’intestino. Di conseguenza, il microbioma svolge un ruolo cruciale nell’educare e modulare il sistema immunitario, distinguendo i patogeni dai batteri benefici (commensali), promuovendo la produzione di anticorpi IgA e mantenendo l’equilibrio tra risposte pro-infiammatorie e anti-infiammatorie.
Quando si verifica, la disbiosi, cioè lo squilibrio del microbioma, può portare a infiammazione cronica di basso grado, aumentando il rischio di malattie autoimmuni, allergie e disturbi metabolici.
Barriera intestinale: la prima linea di difesa
Parallelamente, il microbioma rafforza le tight junctions (giunzioni strette) tra le cellule che costituiscono la parete intestinale. Mantenere l’integrità della barriera intestinale previene il leaky gut (intestino permeabile o “gocciolante”), condizione in cui tossine, batteri e molecole infiammatorie possono passare nel flusso sanguigno, scatenando risposte immunitarie inappropriate.
Asse intestino-cervello: comunicazione bidirezionale
L’asse intestino-cervello rappresenta una delle scoperte più affascinanti della neuroscienza moderna. In particolare, il microbioma comunica con il cervello attraverso multiple vie: il nervo vago rappresenta la principale via nervosa di comunicazione diretta, i metaboliti batterici (SCFAs, neurotrasmettitori come serotonina e GABA, triptofano) agiscono come messaggeri chimici, il sistema immunitario trasmette segnali attraverso citochine e mediatori infiammatori, e il sistema endocrino utilizza ormoni e molecole segnale.
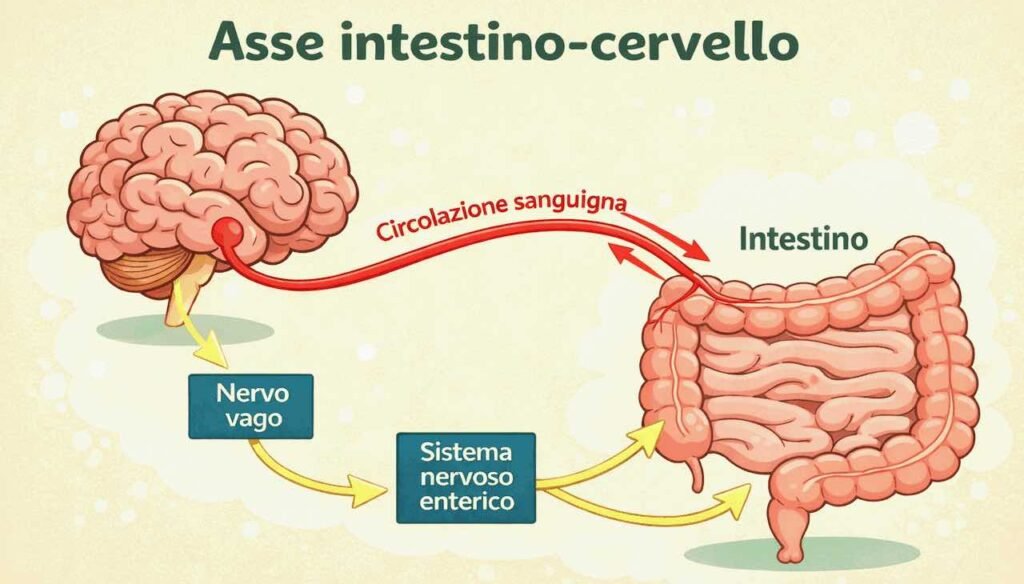
A questo proposito, studi recenti pubblicati nel 2025 su Pharmacological Research hanno confermato in modo definitivo che alterazioni del microbioma sono causalmente associate a disturbi neuropsichiatrici come depressione, ansia, autismo, schizofrenia, disturbi alimentari e disturbi neurocognitivi.
In particolare, la review IUPHAR pubblicata nel 2025 sulla rivista Pharmacological Research, ha evidenziato come il microbioma influenzi la produzione di oltre il 90% della serotonina corporea (principalmente nell’intestino), oltre a GABA, dopamina e altri neurotrasmettitori chiave. Le tecniche avanzate di sequenziamento metagenonico hanno inoltre permesso di identificare specifiche carenze microbiche associate a condizioni come la depressione maggiore, caratterizzate da una riduzione di batteri produttori di butirrato e un aumento di specie pro-infiammatorie.
È importante sottolineare che la comunicazione è profondamente bidirezionale: stress cronico, traumi psicologici e disturbi dell’umore alterano rapidamente la composizione microbica attraverso il rilascio di catecolamine e cortisolo, creando un circolo vizioso che perpetua il disagio mentale.
Pubblicità
Cosa influenza il microbioma intestinale e come prendersene cura
Il microbioma intestinale è un ecosistema dinamico e altamente plastico, che può essere modificato, in meglio o in peggio, lungo tutto l’arco della vita. Di fatto, numerosi fattori ne determinano la composizione e la funzionalità.
Formazione del microbioma nel neonato
Il microbioma inizia a svilupparsi già in utero (influenzato dal microbioma materno), ma la colonizzazione principale avviene alla nascita e nei primi 2-3 anni di vita.
- Il parto vaginale, in particolare, trasmette batteri benefici dalla madre (soprattutto Lactobacillus e Bifidobacterium), favorendo una maggiore diversità iniziale.
- Il parto cesareo, invece, porta a una colonizzazione più lenta e alterata, spesso con minore presenza di Bifidobacterium e maggiore rischio di disbiosi a lungo termine.
- L’allattamento al seno arricchisce ulteriormente il microbiota grazie agli oligosaccaridi del latte umano (HMOs), potenti prebiotici naturali che nutrono selettivamente Bifidobacterium e altri batteri benefici.
Questi primi anni rappresentano, in altre parole, una finestra critica: le abitudini alimentari e lo stile di vita dei genitori in questa fase influenzano la composizione del microbioma per decenni.
Il microbioma nell’adulto
Nell’età adulta il microbioma si è ben formato, ma rimane modificabile: infatti risponde rapidamente a cambiamenti mirati, e, con interventi opportuni, può migliorare già in poche settimane.
Alimentazione: il fattore più potente per modellare il microbioma
Per capire davvero come alcuni alimenti possano influenzare in profondità il nostro intestino, dobbiamo partire da due concetti chiave: prebiotici e probiotici. Sono spesso confusi, ma lavorano in modo complementare e sinergico: i primi nutrono i batteri buoni che già hai, i secondi li aggiungono dall’esterno. Insieme formano la strategia più efficace per mantenere un microbiota diversificato, resiliente e funzionale.
Prebiotici: il “cibo” che nutre i tuoi batteri buoni
I prebiotici sono fibre alimentari non digeribili dall’organismo umano. Resistono agli enzimi digestivi dello stomaco e dell’intestino tenue e raggiungono praticamente intatti il colon, dove fungono da substrato selettivo per i batteri benefici già presenti, in particolare ceppi di Bifidobacterium, Lactobacillus, Faecalibacterium prausnitzii e diverse specie di Roseburia.

I prebiotici, quindi, non introducono nuovi batteri, ma fanno crescere e proliferare quelli “già di casa” nel tuo intestino, migliorando la diversità microbica, rafforzando le tight junctions (giunzioni strette) tra le cellule che costituiscono la parete intestinale, e aumentando la produzione di metaboliti protettivi come gli acidi grassi a catena corta (butirrato, propionato, acetato). Il butirrato, in particolare, è il principale carburante delle cellule del colon, rafforza le la barriera intestinale, riduce l’infiammazione e modula positivamente il sistema immunitario e il metabolismo.
Quanto ne servono?
Le raccomandazioni più aggiornate (EFSA, WHO e consensus 2024-2025) indicano almeno 25–35 g di fibre totali al giorno per un adulto. In Italia la media è ancora bassa (15–18 g/giorno): aumentare le fibre è uno dei cambiamenti più semplici e potenti per la salute intestinale.
I prebiotici più efficaci e le relative fonti
- Inulina e fruttoligosaccaridi (FOS): si trovano in cipolle, aglio, porri, scalogno, topinambur, cicoria, carciofi, asparagi, radicchio, banane poco mature
- Galattoligosaccaridi (GOS): le fonti includono legumi (ceci, lenticchie, fagioli, fave), latte e derivati (in tracce naturali)
- Beta-glucani e pectine: se ne trovano in avena, orzo, mele con buccia, pere, agrumi, semi di lino e chia
L’amido resistente: il prebiotico “nascosto” più potente
Esiste una categoria di prebiotici ancora più potente, ma spesso trascurata: l’amido resistente, che si forma naturalmente quando alcuni alimenti ricchi di amido (come patate, riso e pasta) vengono cotti e poi raffreddati (almeno 12–24 ore in frigorifero). Questo “processo di retrogradazione” rende l’amido indigeribile per noi, ma un ottimo substrato specifico per i batteri produttori di butirrato, con effetti dimostrati su glicemia, sazietà, infiammazione e integrità della barriera intestinale.
Per scoprire tutti i trucchi pratici per massimizzare l’amido resistente nella tua dieta quotidiana, ti consigliamo di leggere la nostra guida completa ai benefici dell’amido resistente.
Probiotici: i i batteri benefici che introduci con l’alimentazione
I probiotici sono microrganismi vivi, principalmente batteri lattici o bifidobatteri, ma anche alcuni lieviti come Saccharomyces boulardii, che, assunti con alimenti o integratori, sono in grado di sopravvivere al passaggio gastrico e di colonizzare temporaneamente l’intestino, portando benefici diretti: modulazione del sistema immunitario, produzione di acidi grassi a catena corta (SCFAs), competizione con patogeni, miglioramento della barriera mucosa.
I ceppi più studiati e efficaci appartengono ai generi Lactobacillus (es. L. rhamnosus, L. casei, L. acidophilus) e Bifidobacterium (es. B. longum, B. bifidum, B. breve), ma sono importanti anche ceppi di Saccharomyces boulardii (lievito) e altri.
Dove trovare i probiotici in modo naturale?
Gli alimenti fermentati non pastorizzati sono la fonte più ricca e biodisponibile di probiotici vivi:
- Yogurt greco naturale o tradizionale (non zuccherato)
- Kefir di latte o acqua
- Crauti non pastorizzati
- Kimchi autentico
- Tempeh
- Miso (non pastorizzato)
- Kombucha artigianale (con basso zucchero residuo)
- Formaggi stagionati non pastorizzati (es. parmigiano, pecorino, gorgonzola naturale)

Nota: i prodotti pastorizzati o molto processati perdono la maggior parte dei probiotici vivi. Scegli sempre versioni “crude” o “vive” indicate in etichetta.
Combinare prebiotici e probiotici: il segreto dell’approccio sinbiotico
Quando prebiotici e probiotici vengono assunti insieme (o quando alimenti naturalmente ricchi di entrambi vengono consumati), si crea un effetto sinbiotico: i probiotici introdotti trovano un ambiente nutrizionale favorevole che ne favorisce sopravvivenza, adesione e attività metabolica nel colon. È proprio questa combinazione che massimizza i benefici osservati negli studi clinici su digestione, immunità, infiammazione e persino benessere mentale.
Esempi pratici:
- Yogurt greco + banana poco matura + semi di chia
- Kefir con avena overnight (fredda 12–24 h)
- Insalata di riso freddo (raffreddato) + crauti + legumi
- Kimchi con patate bollite fredde
Assicurarti 30 g di fibre + fonti di probiotici vivi è una delle strategie più efficaci, naturali e low-cost per supportare il tuo microbioma
Polifenoli: efficaci per la diversità del microbioma intestinale
I polifenoli sono composti vegetali con spiccate proprietà antiossidanti e antinfiammatorie, presenti in molti alimenti di origine vegetale.
Tuttavia, la loro biodisponibilità è generalmente bassa: solo una piccola quota (tipicamente 5–10%) viene assorbita direttamente nell’intestino tenue, in forma di agliconi o dopo idrolisi parziale. La maggior parte (90–95%) sfugge all’assorbimento in questa sede e raggiunge quindi il colon praticamente intatta. È proprio qui, nel colon, che il microbiota intestinale svolge un ruolo fondamentale: attraverso enzimi specifici, i batteri trasformano i polifenoli complessi in metaboliti più piccoli e spesso più bioattivi (come acidi fenolici, urolitine, equolo e valerolattone). Questi metaboliti possono così essere assorbiti nel colon e entrare quindi nella circolazione sistemica, contribuendo agli effetti sistemici sulla salute (anti-infiammatori, cardiovascolari, neuroprotettivi).
Infatti, studi recenti dimostrano che un apporto regolare di polifenoli aumenta significativamente la diversità alfa (ricchezza di specie) e beta (differenze tra individui) del microbiota, favorendo la crescita di generi benefici come Akkermansia muciniphila, Faecalibacterium prausnitzii e alcuni Bifidobacterium, mentre riduce la presenza di specie pro-infiammatorie.
Le fonti alimentari di polifenoli
Tra le fonti alimentari più ricche ed efficaci troviamo i frutti rossi come mirtilli, more, lamponi, ribes e fragole, ricchissimi di antociani. Allo stesso modo, tè verde e tè nero apportano catechine e teaflavine, mentre il cioccolato fondente con almeno 70-85% di cacao fornisce flavonoidi come l’epicatechina. Inoltre, l’olio extravergine d’oliva contiene idrossitirosolo e oleuropeina, e noci e mandorle sono ricche di ellagitannini. Infine, uva rossa, melograno, cacao amaro e spezie come curcuma, cannella e chiodi di garofano completano il quadro.

L’uva rossa (soprattutto varietà come Cabernet Sauvignon, Merlot, Sangiovese, Nebbiolo, Aglianico, Cannonau, Primitivo, Negroamaro, ecc.) contiene elevate quantità di resveratrolo (soprattutto nella buccia), antociani (responsabili del colore rosso-viola), flavonoidi (quercetina, catechine, epicatechine), tannini (proantocianidine), acidi fenolici (acido caffeico, ferulico, p-cumarico).
Di conseguenza, anche un consumo moderato di vino rosso (1 bicchiere al giorno, preferibilmente durante i pasti) contribuisce significativamente all’apporto di polifenoli, grazie alla macerazione prolungata con bucce e vinaccioli. Studi recenti confermano che questa fonte è tra le più efficaci per promuovere Akkermansia e Faecalibacterium, purché non si superino le quantità raccomandate.
L’importanza della diversificazione vegetale
Un dato particolarmente interessante emerge dall’American Gut Project (e dal suo successore British Gut Project), un progetto citizen-science su larga scala condotto coinvolgendo oltre 10.000 cittadini volontari non professionisti provenienti da Stati Uniti, Regno Unito e Australia: i partecipanti che consumavano almeno 30 tipi diversi di vegetali nell’arco di una settimana mostravano un microbioma significativamente più diversificato rispetto a chi ne consumava 10 o meno.
Soprattutto, la varietà vegetale settimanale influenza la diversità microbica più che essere vegani, vegetariani od onnivori. Non è il tipo di dieta a fare la differenza, ma quanti tipi diversi di vegetali consumi. Ogni ortaggio, frutto, legume, cereale integrale, erba o spezia apporta infatti fibre, polifenoli e composti bioattivi unici che nutrono batteri diversi, favorendo una comunità microbica più ricca e stabile.
Alimenti e abitudini da limitare per proteggere il microbioma
Aggiungere prebiotici e probiotici nella dieta, tuttavia, non basta: è altrettanto importante ridurre o eliminare fattori che danneggiano attivamente la diversità e l’equilibrio batterico.
Innanzitutto, zuccheri raffinati e dolcificanti artificiali come aspartame, sucralosio e saccarina alterano rapidamente il microbiota, riducendo la diversità e favorendo specie pro-infiammatorie come Proteobacteria patogeni.
Allo stesso modo, i cibi ultra-processati (snack industriali, bibite zuccherate, cibi pronti), ricchi di emulsionanti, additivi e zuccheri, promuovono infiammazione intestinale e sistemica, leaky gut e dysbiosi.
Inoltre, l’eccesso di carne rossa e soprattutto processata (salumi, wurstel, hamburger industriali) è associato a un aumento di batteri produttori di TMAO (trimetilammina N-ossido) e solfuro di idrogeno, con effetti pro-infiammatori e pro-aterogeni.
Infine, gli antibiotici non necessari o autoprescritti causano una drastica riduzione della diversità microbica, con effetti che possono durare mesi o anni. Per questo motivo, usarli solo quando prescritti dal medico e, se possibile, supportare il recupero con prebiotici e probiotici.
Tabella pratia: alimenti e nemici del microbioma
| CATEGORIA | ALIMENTI BENEFICI ✓ | ALIMENTI DA LIMITARE ✗ |
|---|---|---|
| Fibre Prebiotiche | Cipolle, aglio, porri, legumi, avena, asparagi, carciofi, banane | Zuccheri raffinati, dolcificanti artificiali (riducono diversità) |
| Fermentati | Yogurt greco naturale, kefir, crauti non pastorizzati, kimchi, kombucha, miso | Cibi ultra-processati (promuovono infiammazione) |
| Polifenoli | Frutti rossi, tè verde, cioccolato fondente ≥70%, olio EVO, noci | Eccesso di carne rossa processata (altera equilibrio batterico) |
Un microbioma sano non si costruisce solo integrando correttamente, ma anche eliminando o riducendo drasticamente i fattori che lo destabilizzano. La combinazione di varietà vegetale, polifenoli, prebiotici e probiotici, insieme alla limitazione degli alimenti disruptivi, rappresenta l’approccio più completo e scientificamente provato per nutrire il tuo “secondo cervello” intestinale.
Pubblicità
Stile di vita
La dieta non è l’unico fattore che modella il nostro microbiota intestinale. Lo stile di vita quotidiano esercita un’influenza altrettanto profonda e spesso sottovalutata, agendo attraverso vie neuroendocrine, immunitarie e metaboliche che si intrecciano con l’asse intestino-cervello.
Esercizio fisico regolare
L’attività motoria è uno dei più potenti modulatori naturali della composizione e della diversità microbica. Infatti, studi longitudinali e meta-analisi recenti dimostrano che le persone che praticano esercizio moderato-vigoroso presentano un microbiota più ricco di generi benefici (Akkermansia, Faecalibacterium, Roseburia) e una maggiore produzione di acidi grassi a catena corta (SCFAs), in particolare butirrato.
Le linee guida dell’Organizzazione Mondiale della Sanità (OMS) raccomandano almeno 150 minuti a settimana di attività aerobica moderata (camminata veloce, nuoto, ciclismo leggero, yoga dinamico) o 75 minuti di attività intensa (corsa, HIIT, spinning), più esercizi di forza 2 volte a settimana. Significativamente, chi raggiunge o supera questi livelli mostra non solo una maggiore diversità alfa (ricchezza di specie), ma anche una riduzione dell’infiammazione sistemica e un miglioramento della sensibilità insulinica mediato dal microbiota.
Sonno di qualità
Parallelamente, il ritmo circadiano regola profondamente il microbiota: durante il sonno profondo si verificano processi di riparazione della barriera intestinale, regolazione immunitaria e produzione di metaboliti antinfiammatori.
Dormire regolarmente 7-9 ore per notte, con orari stabili (anche nei weekend), è associato a un microbiota più stabile e diversificato.
Al contrario, privazione cronica di sonno o ritmi irregolari (jet lag sociale, turni notturni) causano disbiosi rapida: aumento di Proteobacteria patogeni, riduzione di Bifidobacterium e Firmicutes benefici, con effetti su umore, appetito e metabolismo.
Gestione dello stress
Infine, lo stress cronico attiva l’asse ipotalamo-ipofisi-surrene, aumentando cortisolo e catecolamine che alterano la motilità intestinale, la permeabilità della mucosa e la composizione batterica. Fortunatamente, tecniche evidence-based come mindfulness, meditazione, yoga, tai chi e respirazione diaframmatica profonda riducono l’impatto negativo sull’asse intestino-cervello, favorendo la crescita di batteri anti-infiammatori e migliorando la resilienza microbica.

In sintesi, esercizio regolare, sonno di qualità e gestione efficace dello stress non sono solo “buone abitudini”: sono modulatori diretti del microbioma, capaci di amplificare o contrastare gli effetti della dieta. Di fatto, chi adotta uno stile di vita equilibrato sotto questi aspetti mostra un microbiota più diversificato e funzionale, con ricadute positive su immunità, metabolismo, umore e longevità.
ATTENZIONE: Questi sono consigli generali basati sulle evidenze scientifiche. Tuttavia, per raccomandazioni personalizzate, soprattutto in presenza di patologie o condizioni specifiche, è fondamentale consultare un medico o un nutrizionista qualificato.
Pubblicità
Prospettive future e frontiere della ricerca
La ricerca sul microbioma intestinale è in continua espansione. Ecco dunque le frontiere più promettenti per il futuro:
Psychobiotics: batteri per la salute mentale
I psychobiotics sono probiotici che, se assunti in quantità adeguate, producono benefici misurabili per la salute mentale modulando l’asse intestino-cervello. In particolare, recenti meta-analisi e review sistematiche hanno evidenziato il loro potenziale clinico nel trattamento di depressione, ansia e disturbi dell’umore.
Ad esempio, ceppi specifici come Lactobacillus helveticus R0052 e Bifidobacterium longum 1714 hanno dimostrato in studi randomizzati controllati di ridurre significativamente i punteggi di ansia e depressione, probabilmente attraverso la modulazione dell’asse HPA (ipotalamo-ipofisi-surrene), la riduzione dei livelli di cortisolo e l’aumento della produzione di GABA e BDNF (fattore neurotrofico cerebrale).
Ancora più interessante, studi di neuroimaging funzionale hanno addirittura mostrato che alcuni psychobiotics possono modificare l’attività di regioni cerebrali coinvolte nell’elaborazione emotiva, come l’amigdala e la corteccia prefrontale.
Sebbene promettenti, tuttavia queste terapie richiedono ancora ulteriori ricerche per standardizzare dosaggi, durata del trattamento e identificare i pazienti che ne beneficerebbero maggiormente.
Postbiotici: oltre probiotici e prebiotici
I postbiotici sono metaboliti e componenti cellulari prodotti dai batteri probiotici (es. SCFAs, peptidi bioattivi) che offrono benefici per la salute senza necessità di batteri vivi. Rappresentano indubbiamente una nuova frontiera terapeutica più stabile e controllabile.
Trapianto di microbiota fecale (FMT)
Il trapianto di microbiota fecale da donatore sano a ricevente sta mostrando efficacia promettente nel trattamento di infezioni ricorrenti da Clostridioides difficile e viene inoltre studiato per malattie infiammatorie intestinali, obesità e disturbi metabolici.
Medicina personalizzata basata sul microbioma
Infine, il sequenziamento del microbioma individuale permetterà interventi nutrizionali e terapeutici personalizzati. L’obiettivo è infatti sviluppare strategie su misura basate sulla composizione microbica unica di ciascun individuo per ottimizzare salute, metabolismo e longevità.
Conclusione: investi nel tuo microbioma, investi nella tua salute
Prendersi cura del microbioma intestinale non è una moda passeggera: è una strategia scientifica evidence-based per migliorare energia, immunità, benessere mentale e longevità. In definitiva, i 38 trilioni di microrganismi che vivono nel tuo intestino sono alleati preziosi per la salute globale.
Questo articolo rappresenta il pilastro introduttivo della serie sul microbioma. Nei prossimi articoli approfondiremo l’asse intestino-cervello e il ruolo del microbioma nella salute mentale, esploreremo inoltre cosa ci insegnano i centenari sul rapporto tra microbioma e longevità, e analizzeremo infine gli psychobiotics come interventi mirati per ansia e depressione.
Pubblicità
Riferimenti Scientifici
Tutti i riferimenti rimandano a studi peer-reviewed su PubMed:
1. Definizione, composizione e ruolo generale del microbioma nella salute umana
Queste review trattano cos’è il microbioma, la sua composizione, il ruolo come organo metabolico ed inoltre il legame con nutrizione/salute globale.
- Valencia, S., Bordiga, M., & Randeni, N. (2025). Human gut microbiome: A connecting organ between nutrition, metabolism, and health. International Journal of Molecular Sciences, 26(9), Article 4112. https://doi.org/10.3390/ijms26094112Link PubMed:https://pubmed.ncbi.nlm.nih.gov/40362352
- Sanz, Y., & others. (2025). The gut microbiome connects nutrition and human health. Nature Reviews Gastroenterology & Hepatology, 22(8), 534–555. https://doi.org/10.1038/s41575-025-01077-5Link PubMed:https://pubmed.ncbi.nlm.nih.gov/40468006
- Van Hul, M., Eeckhaut, V., Falony, G., & De Vos, W. M. (2024). What defines a healthy gut microbiome? Gut, 73(11), 1893–1908. https://doi.org/10.1136/gutjnl-2024-333378Link PubMed:https://pubmed.ncbi.nlm.nih.gov/39322314
- Paul, J. K., et al. (2025). Unlocking the secrets of the human gut microbiota: Comprehensive review on its role in different diseases. World Journal of Gastroenterology, 31(5), Article 99913. https://doi.org/10.3748/wjg.v31.i5.99913Link PubMed:https://pubmed.ncbi.nlm.nih.gov/39926224
2. Sviluppo precoce del microbioma (early-life)
Focus sulla colonizzazione iniziale e impatti a lungo termine.
- Borrego-Ruiz, A., et al. (2025). Early-life gut microbiome development and its potential long-term impact on health outcomes. Microbiome Research Reports, 4(2), Article 20. https://doi.org/10.20517/mrr.2024.78Link PubMed:https://pubmed.ncbi.nlm.nih.gov/40852125
3. Interazione con il sistema immunitario
Ruolo del microbioma nell’educazione immunitaria e prevenzione infiammazione.
- Ghosh, N., & World J Gastrointest Pathophysiol. (2025). Guardians within: Cross-talk between the gut microbiome and host immune system. World Journal of Gastrointestinal Pathophysiology, 16(4), Article 111245. https://doi.org/10.4291/wjgp.v16.i4.111245Link PubMed:https://pubmed.ncbi.nlm.nih.gov/41479870
4. Metaboliti (SCFAs) e loro effetti sulla salute
Ruolo degli acidi grassi a catena corta nella salute e malattia.
- Hays, K. E., et al. (2024). The interplay between gut microbiota, short-chain fatty acids, and implications for host health and disease. Gut Microbes, 16(1), Article 2393270. https://doi.org/10.1080/19490976.2024.2393270Link PubMed:https://pubmed.ncbi.nlm.nih.gov/39284033
- Mukhopadhya, I., et al. (2025). Gut microbiota-derived short-chain fatty acids and their role in human health and disease. Nature Reviews Microbiology, 23(10), 635–651. https://doi.org/10.1038/s41579-025-01183-wLink PubMed:https://pubmed.ncbi.nlm.nih.gov/40360779
5. Asse intestino-cervello (gut-brain axis)
Comunicazione bidirezionale e ruolo in disturbi neuropsichiatrici/neurodegenerativi.
- Lee, S.-H., & others. (2025). IUPHAR review: Microbiota-gut-brain axis and its role in neuropsychiatric disorders. Pharmacological Research, 216, Article 107749. https://doi.org/10.1016/j.phrs.2025.107749Link PubMed:https://pubmed.ncbi.nlm.nih.gov/40306604
- Loh, J. S., et al. (2024). Microbiota-gut-brain axis and its therapeutic applications in neurodegenerative diseases. Signal Transduction and Targeted Therapy, 9(1), Article 37. https://doi.org/10.1038/s41392-024-01743-1Link PubMed:https://pubmed.ncbi.nlm.nih.gov/38360862
6. Influenza dello stile di vita sul microbioma
Dieta, esercizio, sonno, stress e fattori ambientali.
- Zeng, Q., et al. (2025). The human gut microbiota is associated with host lifestyle: A comprehensive narrative review. Frontiers in Microbiology, 16, Article 1549160. https://doi.org/10.3389/fmicb.2025.1549160Link PubMed:https://pubmed.ncbi.nlm.nih.gov/40625617
7. Interventi pratici (probiotici, prebiotici, sinbiotici, postbiotici)
Modulazione del microbioma tramite interventi nutrizionali e terapeutici.
- Kim, Y.-T., Mills, D. A., & Kim, Y.-T. (2024). Exploring the gut microbiome: Probiotics, prebiotics, synbiotics, and postbiotics as key players in human health and disease improvement. Food Science and Biotechnology, 33(9), 2065–2080. https://doi.org/10.1007/s10068-024-01620-1Link PubMed:https://pubmed.ncbi.nlm.nih.gov/39130661
- Lee, Y. T., et al. (2025). Impacts of lifestyle and microbiota-targeted interventions for overweight and obesity on the human gut microbiome: A systematic review. Obesity Reviews. Advance online publication. https://doi.org/10.1111/obr.70037Link PubMed:https://pubmed.ncbi.nlm.nih.gov/41372103 (nota: il PMID 41372103 sembra riferirsi a un contesto simile, ma verifica l’abstract per conferme esatte sul titolo)
8. Postbiotici e psychobiotics
Interventi innovativi per neurodegenerazione e depressione.
Śliwka, A., & others. (2025). Psychobiotics in depression: Sources, metabolites, and treatment—A systematic review. Nutrients, 17(13), Article 2139. https://doi.org/10.3390/nu17132139Link PubMed:https://pubmed.ncbi.nlm.nih.gov/40647242
Gupta, M. K., et al. (2025). Innovative interventions: Postbiotics and psychobiotics in neurodegenerative disease treatment. Probiotics and Antimicrobial Proteins. Advance online publication. https://doi.org/10.1007/s12602-025-10632-0Link PubMed:https://pubmed.ncbi.nlm.nih.gov/40576748
Pubblicità
Pubblicità