Eccoci al secondo appuntamento della nostra serie dedicata alla terapia del diabete mellito. Dopo aver analizzato il ruolo insostituibile dell’insulina nel trattamento del diabete di tipo 1, oggi punteremo i riflettori verso uno dei pilastri terapeutici più rivoluzionari della medicina moderna: la Metformina, farmaco di prima scelta per il diabete di tipo 2 che ha trasformato l’approccio terapeutico a questa patologia.
Il nostro viaggio proseguirà poi esplorando due famiglie di farmaci che condividono un meccanismo d’azione tanto elegante quanto diretto: Sulfaniluree e Glinidi, molecole capaci di dialogare direttamente con le cellule Beta pancreatiche per stimolarle alla secrezione di insulina.
- La Metformina
- Come agisce la Metformina?
- Il metabolismo energetico cellulare: le basi fisiologiche
- Inibizione del complesso I mitocondriale e conseguente attivazione dell’AMPK (Figura 1)
- Altri effetti della Metformina non legati all’attivazione di AMPK
- Efficacia clinica della Metformina
- I principali vantaggi della Metformina (Fig. 4)
- Possibili effetti collaterali e controindicazioni della Metformina (Figura 5)
- Posologia e formulazioni disponibili
- Un pilastro della terapia moderna
- Sulfaniluree e Glinidi: stimolatori della secrezione insulinica
- Il Nostro Viaggio non Finisce Qui…
- Bibliografia
La Metformina
La Metformina è considerata da decenni il farmaco di riferimento per il trattamento del diabete di tipo 2. Appartiene alla famiglia delle biguanidi ed è uno dei medicinali più studiati, sicuri ed efficaci nella storia della medicina moderna.
Viene generalmente prescritta come prima scelta terapeutica dopo la diagnosi, in associazione alle modifiche dello stile di vita. Il suo utilizzo è supportato da un’enorme mole di dati clinici, accumulati in oltre 60 anni di esperienza.
Come agisce la Metformina?
Il meccanismo d’azione della Metformina è complesso e multifattoriale, ed in molti aspetti non completamente chiarito. Agisce su diversi livelli del metabolismo, motivo per cui è così efficace e ben tollerata. Andiamo con ordine.
Il metabolismo energetico cellulare: le basi fisiologiche
Per comprendere appieno il meccanismo d’azione della Metformina, è fondamentale partire dalle basi del metabolismo energetico cellulare. Ogni cellula del nostro organismo necessita di energia per svolgere le proprie funzioni vitali, dalla sintesi proteica al trasporto di molecole attraverso le membrane cellulari.
L’energia cellulare è immagazzinata principalmente sotto forma di adenosina trifosfato (ATP), una molecola che rappresenta la “valuta energetica” universale delle cellule. L’ATP è costituita da una base azotata (adenosina) legata a tre gruppi fosfato attraverso legami fosforici ad alta energia. Quando la cellula ha bisogno di energia per i suoi processi metabolici, l’ATP viene idrolizzato: il legame tra il secondo e il terzo gruppo fosfato viene rotto, trasformando l’ATP in adenosina difosfato (ADP) e rilasciando una considerevole quantità di energia. Se il fabbisogno energetico persiste, può verificarsi una seconda idrolisi che converte l’ADP in adenosina monofosfato (AMP), liberando ulteriore energia.
I mitocondri, organelli specializzati presenti nel citoplasma cellulare, si occupano di rigenerare continuamente l’ATP attraverso un processo altamente efficiente chiamato catena respiratoria mitocondriale o catena di trasporto degli elettroni. Questo sistema riallaccia i legami fosforici, convertendo ADP e AMP nuovamente in ATP, garantendo così un rifornimento costante di energia alla cellula.
Inibizione del complesso I mitocondriale e conseguente attivazione dell’AMPK (Figura 1)
1. Azione della Metformina sui mitocondri
La Metformina esercita la sua azione terapeutica interferendo proprio con questo delicato equilibrio energetico. Il farmaco inibisce selettivamente il complesso I della catena respiratoria mitocondriale, un componente chiave del sistema di produzione dell’ATP. Questa inibizione, seppur lieve, determina una riduzione della produzione di ATP all’interno delle cellule.
La conseguenza immediata di questa interferenza è un aumento del rapporto AMP/ATP e ADP/ATP intracellulare. In altre parole, si crea una condizione di relativo deficit energetico cellulare, con accumulo delle forme “scariche” dei nucleotidi adenilici (AMP e ADP) rispetto alla forma “carica” (ATP).
Questa lieve “crisi energetica” indotta dalla Metformina non rappresenta un danno per la cellula, ma piuttosto l’innesco di una cascata di eventi metabolici altamente coordinata e benefica per l’organismo.
2. Attivazione dell’AMPK (AMP-activated protein kinase): il sensore metabolico centrale
Il cambiamento nel rapporto AMP/ATP viene immediatamente percepito dall’AMPK (AMP-activated protein kinase), una chinasi serina/treonina “altamente conservata” (cioè con struttura, funzione e sequenza genica molto simili in diverse specie anche molto lontane evolutivamente – dai lieviti agli esseri umani – e questo ne sottolinea l’importanza biologica essenziale nelle cellule).
L’AMPK agisce come un vero e proprio sensore intracellulare dello stato energetico. Quando rileva un aumento del rapporto AMP/ATP o ADP/ATP, indicativo di una condizione di deficit energetico, si attiva immediatamente per ripristinare l’equilibrio metabolico attraverso un duplice meccanismo:
2.1 Inibizione dei processi anabolici ad alto consumo energetico
L’AMPK attivata blocca selettivamente i processi metabolici che richiedono un elevato dispendio di ATP:
- Lipogenesi: attraverso l’inibizione dell’acetil-CoA carbossilasi 1 (ACC1), l’AMPK riduce la sintesi di acidi grassi e la formazione di tessuto adiposo
- Gluconeogenesi epatica: mediante l’inibizione del complesso TORC2/PGC-1α, viene ridotta la produzione endogena di glucosio da parte del fegato
- Sintesi proteica: attraverso l’inibizione del complesso mTORC1, viene limitata la sintesi di nuove proteine
2.2 Stimolazione dei processi catabolici che generano ATP
Contemporaneamente, l’AMPK promuove i processi metabolici che producono energia:
- Ossidazione degli acidi grassi: viene favorita la “combustione” dei lipidi per produrre ATP
- Uptake di glucosio: attraverso la traslocazione del trasportatore GLUT4, viene aumentato l’assorbimento cellulare di glucosio
- Autofagia: viene stimolato il processo di “riciclaggio” cellulare che degrada componenti danneggiati per recuperare energia e materiali da costruzione
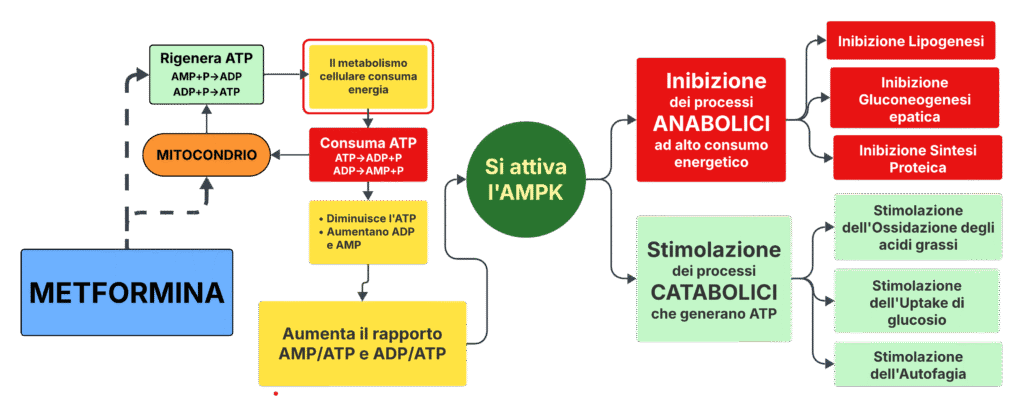
Figura 1 – Meccanismo d’azione della Metformina a livello mitocondriale
Ricapitolando, la Metformina ha la capacità di inibire leggermente la catena respiratoria mitocondriale, il che, determinando un aumento del rapporto AMP/ATP, attiva l’AMPK. Questo porta, come visto, ad una soppressione della gluconeogenesi epatica, ad un miglioramento della sensibilità insulinica e alla modulazione del metabolismo lipidico, contribuendo all’effetto antidiabetico del farmaco.
3. Effetti finali dell’attivazione dell’AMPK
L’attivazione dell’AMPK da parte della Metformina, come detto, ha come risultato finale l’attivazione di diversi meccanismi molecolari, che agiscono sia direttamente sulla sensibilità cellulare all’insulina, sia indirettamente sulla glicemia modulando l’infiammazione.
3.1 A livello muscolare e adiposo
3.1.1 Stimola la traslocazione di GLUT4 sulla membrana cellulare
GLUT4 (Glucose Transporter type 4) è un trasportatore di glucosio presente specificamente nei tessuti insulino-sensibili e cioè nei muscoli scheletrico e cardiaco e nel tessuto adiposo. Si tratta di un carrier transmembrana che consente al glucosio di entrare nella cellula per diffusione facilitata (non attiva). In condizioni basali, è conservato in vescicole intracellulari (GLUT4 Storage Vesicles, GSVs), e non è visibile sulla membrana plasmatica.
Quando l’insulina attiva la via IRS‑1 → PI3K → Akt, viene fosforilato AS160, e questa cascata di eventi determina la fusione delle vescicole contenenti GLUT4 con la membrana cellulare e aumenta così l’assorbimento di glucosio. (Fig. 2)
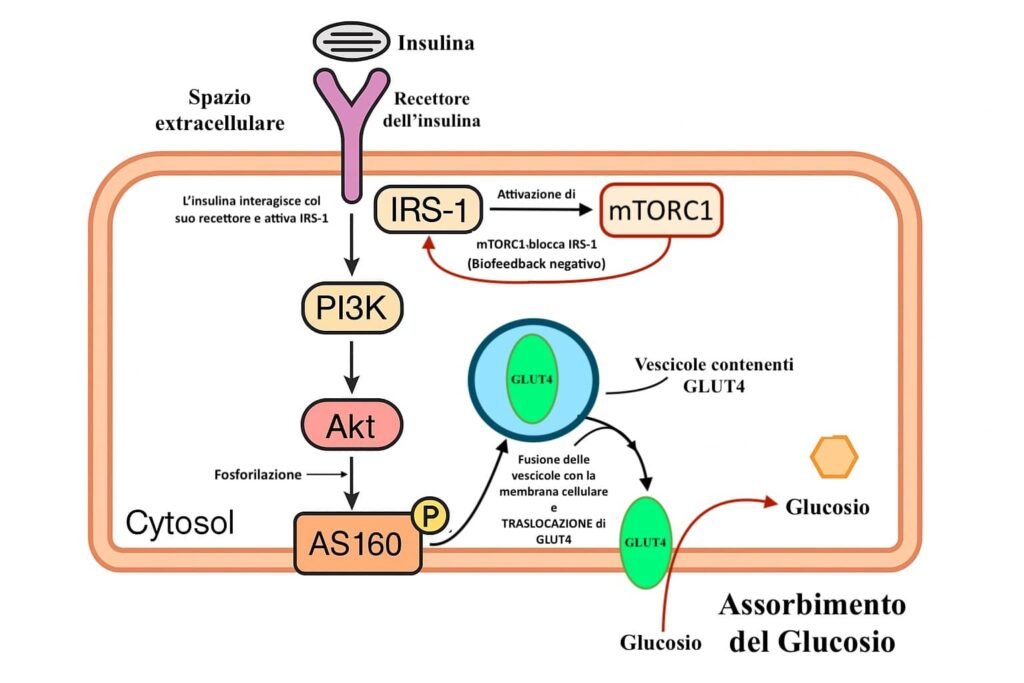
Figura 2 – Traslocazione di GLUT4 e Biofeedback negativo di mTORK1
Analogamente, l’attivazione di AMPK (in presenza di basso ATP, come per l’azione della Metformina, oppure durante l’esercizio fisico) stimola GLUT4 via fosforilazione alternativa di AS160, permettendo l’ingresso di glucosio indipendentemente dall’insulina.
Questo doppio meccanismo (insulina + AMPK) assicura un’efficace captazione di glucosio nei tessuti periferici e migliora la sensibilità insulinica.
Il malfunzionamento di GLUT4 o della sua traslocazione è implicato nell’insulino-resistenza (come appunto nel diabete tipo 2). La Metformina, quindi, in questo frangente stimola l’attività di GLUT4 per mezzo dell’attivazione di AMPK.
3.1.2 Inibisce il Complesso mTORC1 e la sua interazione con IRS-1
Il complesso mTORC1 è un complesso enzimatico che regola la crescita cellulare promuovendo l’anabolismo cellulare, cioè la sintesi proteica e la sintesi lipidica, e inibendo l’autofagia, in risposta a nutrienti, energia e segnali ormonali.
IRS-1 (Insulin Receptor Substrate 1), a sua volta. è una proteina citoplasmatica di segnalazione centrale nella trasduzione del segnale insulinico. Non è un recettore in senso classico (cioè non lega un ligando): una volta attivato dal recettore dell’insulina, trasmette il segnale verso le vie PI3K–Akt e, tra le altre, verso mTORC1.
Quando mTORC1 si attiva, fosforila in modo inibitorio (cioè blocca) la proteina IRS-1 (Insulin Receptor Substrate-1), compromettendo la trasmissione del segnale insulinico, e questo è un meccanismo fisiologico di autoregolazione della risposta insulinica (Biofeedback negativo), che altrimenti andrebbe avanti indefinitivamente. (Fig.2)
Tuttavia, quando mTORC1 è iperattivato in modo cronico, questa retroazione diventa dannosa, portando a una riduzione della sensibilità all’insulina e contribuendo allo sviluppo dell’insulino-resistenza. AMPK, la cui attivazione è promossa dalla Metformina, inibisce mTORC1, riducendo questa retroazione negativa. In questo modo, AMPK favorisce l’efficienza del segnale insulinico, prevenendo l’insulino-resistenza indotta da iperattività mTORC1. (Fig. 3)
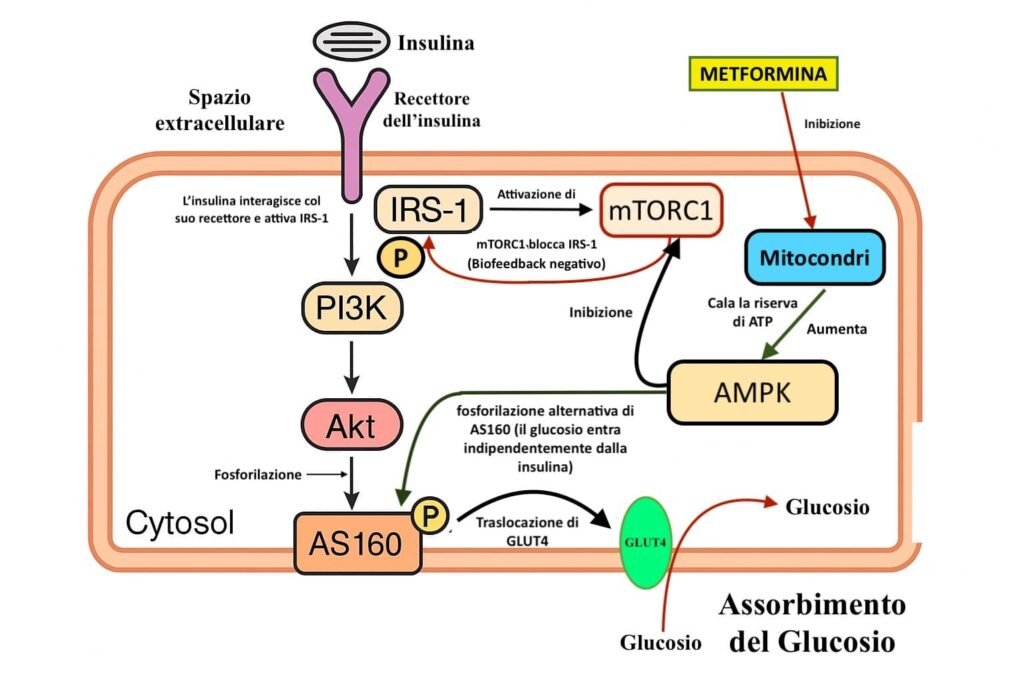
Figura 3 – Meccanismo di azione della Metformina tramite AMPK
3.2 A livello epatico
L’AMPK nel fegato agisce principalmente riducendo la produzione di glucosio (gluconeogenesi) e diminuendo l’accumulo di grassi. Questo aiuta a prevenire la lipotossicità, cioè il danno causato dall’eccesso di lipidi nel fegato, che altrimenti favorirebbe l’insulino-resistenza.
In dettaglio, AMPK abbassa l’attività di enzimi chiave della gluconeogenesi come PEPCK e G6Pase, non solo direttamente, ma anche riducendo l’attivazione di fattori di trascrizione come CREB e PGC-1α, che normalmente aumentano la produzione di questi enzimi.
In sintesi: AMPK, la cui attivazione è favorita farmacologicamente dalla Metformina, spegne la “fabbrica” del glucosio e limita il grasso epatico, migliorando così la sensibilità insulinica.
3.3 A livello sistemico
L’AMPK esercita un’importante azione lipocito-protettiva riducendo l’accumulo intracellulare di lipidi bioattivi come ceramidi e diacilgliceroli (DAG), molecole che normalmente interferiscono con la corretta trasmissione del segnale insulinico a livello cellulare, contribuendo così al mantenimento della sensibilità insulinica dei tessuti.
3.4 Modulazione delle vie infiammatorie e dello stress ossidativo
L’AMPK agisce anche come modulatore antinfiammatorio e antiossidante:
3.4.1 Inibizione dell’infiammazione
L’AMPK svolge un ruolo cruciale nel controllo dell’infiammazione attraverso diversi meccanismi coordinati.
Innanzitutto, inibisce il fattore di trascrizione NF-κB, considerato l’elemento chiave dell’infiammazione cronica, bloccando così la produzione di citochine pro-infiammatorie come TNF-α e IL-6.
Contemporaneamente, l’AMPK favorisce la trasformazione dei macrofagi (cellule del sistema immunitario) in una forma più “calma” e anti-infiammatoria, detta fenotipo M2, capace di riparare i tessuti e risolvere l’infiammazione, in contrapposizione al fenotipo M1 dei macrofagi pro-infiammatori che attaccano e distruggono, utili nelle infezioni ma dannosi se cronicamente attivi.
Inoltre, questa proteina chinasi riduce l’attivazione dell’inflammasoma NLRP3, un complesso molecolare che funge da “sistema d’allarme” cellulare: limitandone l’attivazione, l’AMPK diminuisce la produzione di mediatori infiammatori potenti come l’interleuchina-1β, proteggendo i tessuti dai danni associati all’infiammazione cronica.
3.4.2 Azione antiossidante:
L’AMPK esercita un’azione antiossidante multiforme e coordinata a livello cellulare.
Promuove la mitofagia, un processo di autofagia specializzato che elimina selettivamente i mitocondri danneggiati e disfunzionali, principali fonti di stress ossidativo cellulare.
Parallelamente, attiva il fattore di trascrizione Nrf2, che rappresenta il fattore di controllo primario della risposta antiossidante cellulare, poiché coordina l’attivazione di numerosi geni coinvolti nella difesa contro lo stress ossidativo. Questo fattore di trascrizione agisce come un interruttore molecolare che, una volta attivato, innesca una cascata di eventi che porta alla produzione di enzimi antiossidanti e proteine detossificanti, come la superossido dismutasi (SOD), la catalasi e la glutatione perossidasi, fungendo quindi da coordinatore centrale della risposta protettiva cellulare.
Inoltre, l’AMPK riduce direttamente la produzione di specie reattive dell’ossigeno (ROS) a livello mitocondriale, modulando il flusso elettronico nel complesso I della catena respiratoria.
Questo triplice meccanismo d’azione consente all’AMPK di mantenere l’equilibrio redox cellulare, proteggendo le cellule dai danni ossidativi che caratterizzano molte patologie metaboliche e degenerative, che vengono così influenzate positivamente dall’azione della Metformina.
Altri effetti della Metformina non legati all’attivazione di AMPK
Sebbene l’attivazione dell’AMPK rappresenti un meccanismo centrale nell’azione della Metformina, non tutti gli effetti terapeutici di questo farmaco dipendono esclusivamente da questa via. La ricerca ha infatti identificato diversi meccanismi AMPK-indipendenti che contribuiscono al suo profilo farmacologico.
Tra questi, la modulazione del microbiota intestinale emerge come un’area di crescente interesse: studi recenti dimostrano che la Metformina può alterare favorevolmente la composizione della flora batterica, influenzando positivamente il metabolismo e la risposta glicemica. Inoltre, il farmaco potenzia indirettamente l’azione del GLP-1, un ormone intestinale che stimola la secrezione insulinica in modo glucosio-dipendente e aumenta la sazietà, migliorando ulteriormente il controllo metabolico.
Efficacia clinica della Metformina
La Metformina dimostra un’efficacia clinica consolidata nel controllo glicemico, riducendo l’emoglobina glicata (HbA1c) in modo significativo con diminuzioni tipicamente comprese tra l’1% e il 2%, risultato particolarmente evidente nelle fasi iniziali della malattia quando la funzione delle cellule beta pancreatiche è ancora preservata.
I benefici della Metformina si estendono ben oltre il semplice controllo metabolico, come dimostrato dal prestigioso studio UKPDS (United Kingdom Prospective Diabetes Study), uno dei più influenti trial sulla storia naturale del diabete. Questo studio ha documentato che nei pazienti in sovrappeso con diabete tipo 2, la Metformina ha prodotto una riduzione del 36% della mortalità totale e del 39% del rischio di infarto miocardico, evidenziando un effetto cardioprotettivo che va oltre il controllo glicemico.
Emerge inoltre un potenziale oncologico della Metformina: studi osservazionali hanno rilevato una riduzione dell’incidenza di alcuni tipi di tumore nei pazienti trattati con questo farmaco. Tale effetto antitumorale potrebbe essere mediato dalla modulazione della via mTOR (mechanistic target of rapamycin), un importante regolatore del metabolismo cellulare che controlla crescita, proliferazione e sopravvivenza cellulare, processi cruciali nello sviluppo neoplastico.
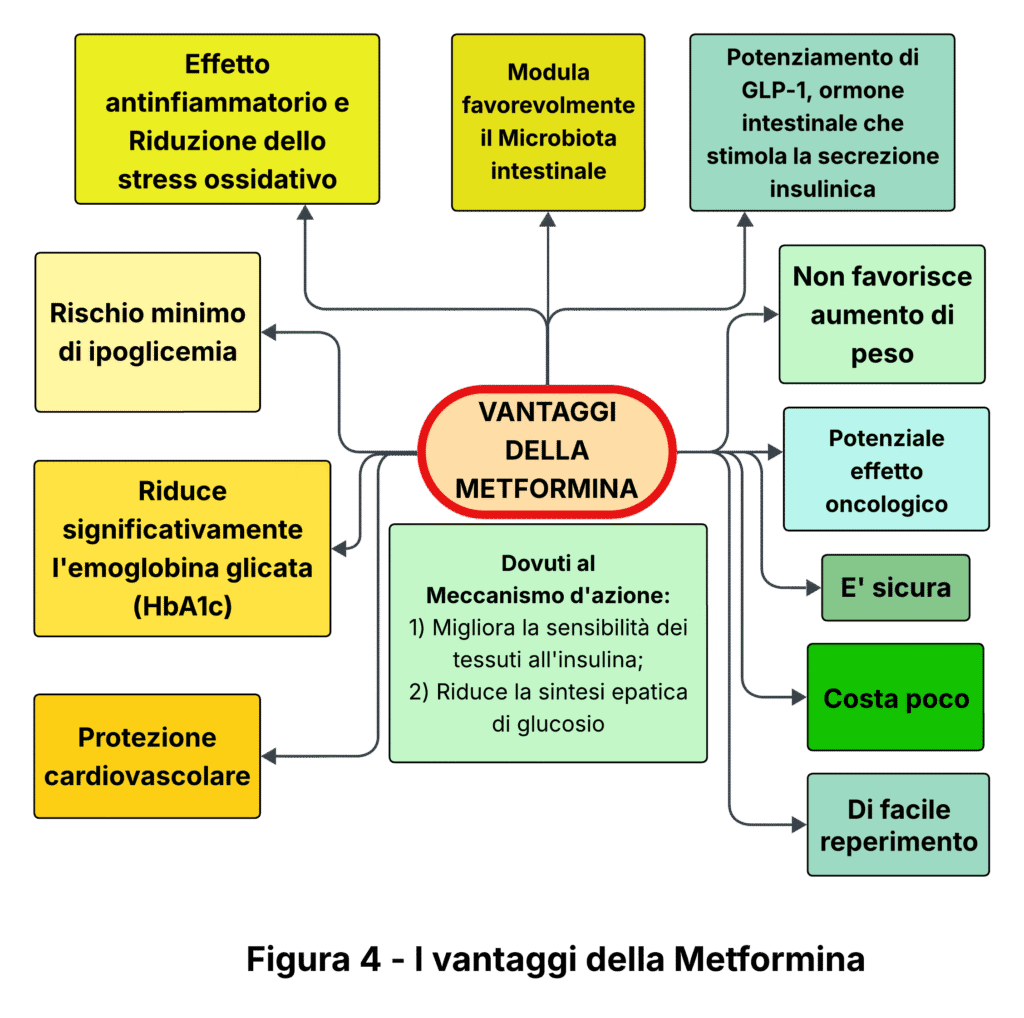
I principali vantaggi della Metformina (Fig. 4)
La Metformina presenta caratteristiche uniche che la distinguono dagli altri farmaci antidiabetici, rendendola particolarmente sicura ed efficace nel trattamento del diabete di tipo 2.
Il principale vantaggio della Metformina risiede nel suo meccanismo d’azione: a differenza di altri farmaci che stimolano direttamente la produzione di insulina, la Metformina agisce principalmente migliorando la sensibilità dei tessuti all’insulina e riducendo la produzione epatica di glucosio. Questo approccio indiretto comporta un rischio di ipoglicemia praticamente nullo quando viene utilizzata in monoterapia, rappresentando un significativo vantaggio in termini di sicurezza per il paziente.
Un altro aspetto fondamentale riguarda l’impatto sul peso corporeo. Mentre molti farmaci antidiabetici, come le sulfaniluree o l’insulina, possono causare un aumento ponderale indesiderato, la Metformina mantiene il peso stabile o può addirittura favorire una modesta riduzione, particolare vantaggiosa per i pazienti diabetici che spesso presentano problemi di sovrappeso.
La Metformina offre inoltre benefici che vanno oltre il controllo glicemico. Gli studi clinici hanno dimostrato che questo farmaco riduce significativamente il rischio di eventi cardiovascolari, che costituiscono la principale causa di mortalità nei pazienti diabetici. Questa protezione cardiovascolare rappresenta un valore aggiunto importante nella gestione complessiva della patologia.
L’accessibilità economica costituisce un ulteriore punto di forza: disponibile come farmaco generico, la Metformina è economica e facilmente reperibile, garantendo continuità terapeutica anche a pazienti con limitate risorse economiche.
Infine, la lunga esperienza clinica di oltre sessant’anni ha fornito solide evidenze sulla sicurezza a lungo termine del farmaco, consolidando la sua posizione come terapia di prima linea nel diabete di tipo 2.
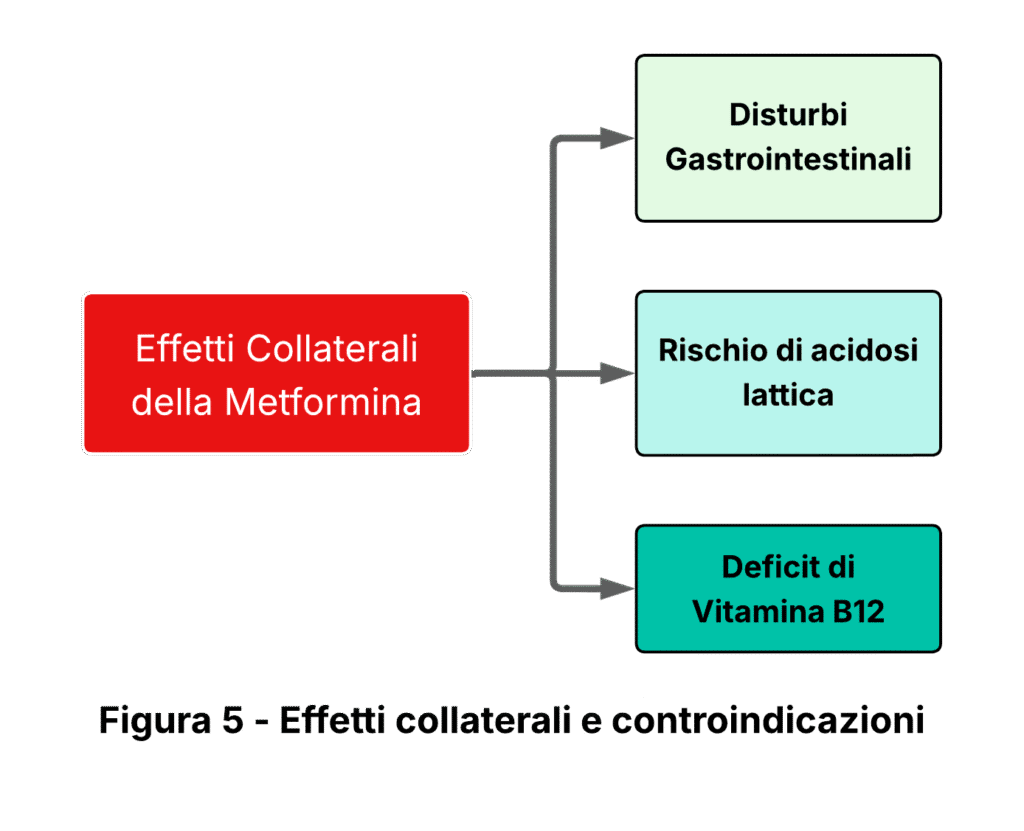
Possibili effetti collaterali e controindicazioni della Metformina (Figura 5)
I disturbi gastrointestinali causati dalla Metformina
I disturbi gastrointestinali rappresentano la categoria di effetti collaterali più comune associata all’uso della Metformina. Nausea, diarrea, crampi addominali e un caratteristico sapore metallico in bocca colpiscono una significativa percentuale di pazienti, manifestandosi tipicamente nelle prime settimane di trattamento. Questa sintomatologia, seppur fastidiosa, presenta un andamento favorevole: l’intensità tende infatti a diminuire progressivamente con la continuazione della terapia, grazie all’adattamento dell’organismo al farmaco. Per minimizzare questi disagi, i clinici spesso prescrivono formulazioni a rilascio prolungato, che garantiscono un rilascio graduale del principio attivo e risultano significativamente meglio tollerate dal tratto gastrointestinale.
L’acidosi lattica da Metformina
Il rischio di acidosi lattica costituisce invece una complicanza rara ma di estrema gravità clinica. Con un’incidenza di circa 0,03 casi ogni 1000 pazienti per anno, questa condizione può rivelarsi potenzialmente fatale se non riconosciuta tempestivamente.
L’acidosi lattica si sviluppa prevalentemente quando l’eliminazione renale della Metformina risulta compromessa, creando un accumulo del farmaco nell’organismo.
Le situazioni cliniche che predispongono a questa complicanza includono l’insufficienza renale grave con filtrato glomerulare inferiore a 30 ml/min, l’insufficienza epatica, lo scompenso cardiaco severo, condizioni di ipossia cronica come la broncopneumopatia cronica ostruttiva in fase avanzata, e il consumo eccessivo di alcool.
La prevenzione rimane l’arma più efficace: un’attenta valutazione della funzionalità renale prima dell’inizio del trattamento e controlli periodici durante la terapia rappresentano elementi fondamentali della gestione clinica.
La carenza di vitamina B12 causata dalla Metformina
L’uso prolungato della Metformina, particolarmente oltre i quattro-cinque anni di trattamento continuativo, può interferire con l’assorbimento intestinale della vitamina B12. Questo fenomeno si verifica attraverso un meccanismo che coinvolge il fattore intrinseco e il complesso vitamina B12-calcio a livello dell’ileo terminale. La carenza di vitamina B12 può manifestarsi con sintomi neurologici e anemia megaloblastica, rendendo necessario un monitoraggio periodico dei livelli ematici di questa vitamina nei pazienti sottoposti a terapia cronica con Metformina. La supplementazione vitaminica può essere facilmente implementata quando necessario, prevenendo le complicanze associate alla carenza.
Posologia e formulazioni disponibili
Dosaggio standard
Il dosaggio standard della Metformina presenta una notevole flessibilità terapeutica, con dosi giornaliere che oscillano tra 500 mg e 2550 mg, distribuite tipicamente in due o tre somministrazioni quotidiane. Questa variabilità posologica consente al clinico di personalizzare il trattamento in base alle specifiche esigenze metaboliche del paziente e alla sua tollerabilità individuale.
Formulazioni a rilascio immediato
Le formulazioni a rilascio immediato rappresentano la tipologia più diffusa sul mercato farmaceutico e necessitano di assunzioni multiple nell’arco della giornata, solitamente concentrate ai pasti principali come colazione e cena. Questa modalità di somministrazione favorisce un controllo glicemico più uniforme durante le ore diurne, sebbene richieda una maggiore aderenza terapeutica da parte del paziente.
Formulazioni a rilascio prolungato (XR o SR)
Le formulazioni a rilascio prolungato, identificate dalle sigle XR (Extended Release) o SR (Sustained Release), rappresentano un’evoluzione tecnologica significativa nella farmacologia della Metformina. Queste preparazioni consentono una somministrazione unica giornaliera, offrendo il duplice vantaggio di migliorare considerevolmente la tollerabilità gastrointestinale e di semplificare il regime terapeutico. Tale caratteristica le rende particolarmente indicate per i pazienti che manifestano sensibilità gastrointestinale alle formulazioni tradizionali.
Formulazioni combinate
Un aspetto particolarmente interessante del panorama terapeutico attuale è rappresentato dalle formulazioni combinate, dove la Metformina viene associata in combinazione fissa con diversi altri farmaci antidiabetici. Queste associazioni includono DPP-4 inibitori, SGLT2 inibitori e sulfaniluree, creando sinergie terapeutiche che permettono di semplificare significativamente la gestione farmacologica del diabete tipo 2. La combinazione fissa non solo riduce il numero di compresse da assumere quotidianamente, ma migliora anche l’aderenza terapeutica del paziente, fattore cruciale per il successo del controllo glicemico a lungo termine.
Un pilastro della terapia moderna
La Metformina rimane il fondamento del trattamento del diabete tipo 2 in tutto il mondo. Anche quando la malattia richiede farmaci aggiuntivi, la Metformina viene spesso mantenuta per la sua efficacia, sicurezza e basso costo. È un esempio eccellente di farmaco ben progettato, ancora attuale dopo oltre mezzo secolo di utilizzo clinico.
Sulfaniluree e Glinidi: stimolatori della secrezione insulinica
Questi farmaci agiscono stimolando direttamente le cellule beta del pancreas a secernere insulina.
Meccanismo d’azione
Il meccanismo d’azione delle sulfoniluree e dei glinidi a livello delle cellule beta pancreatiche rappresenta un processo biologico complesso che coinvolge diversi sistemi di trasporto ionico e cascate di segnalazione intracellulare. (Fig. 6)
La sequenza di eventi inizia con l‘interazione farmaco-recettore sui canali KATP, strutture proteiche fondamentali per la regolazione del potenziale di membrana cellulare.
Il primo step del meccanismo prevede il legame specifico delle sulfoniluree ai recettori SUR1 (Sulfonylurea Receptor 1), subunità regolatrice dei canali KATP presenti sulla membrana delle cellule beta.
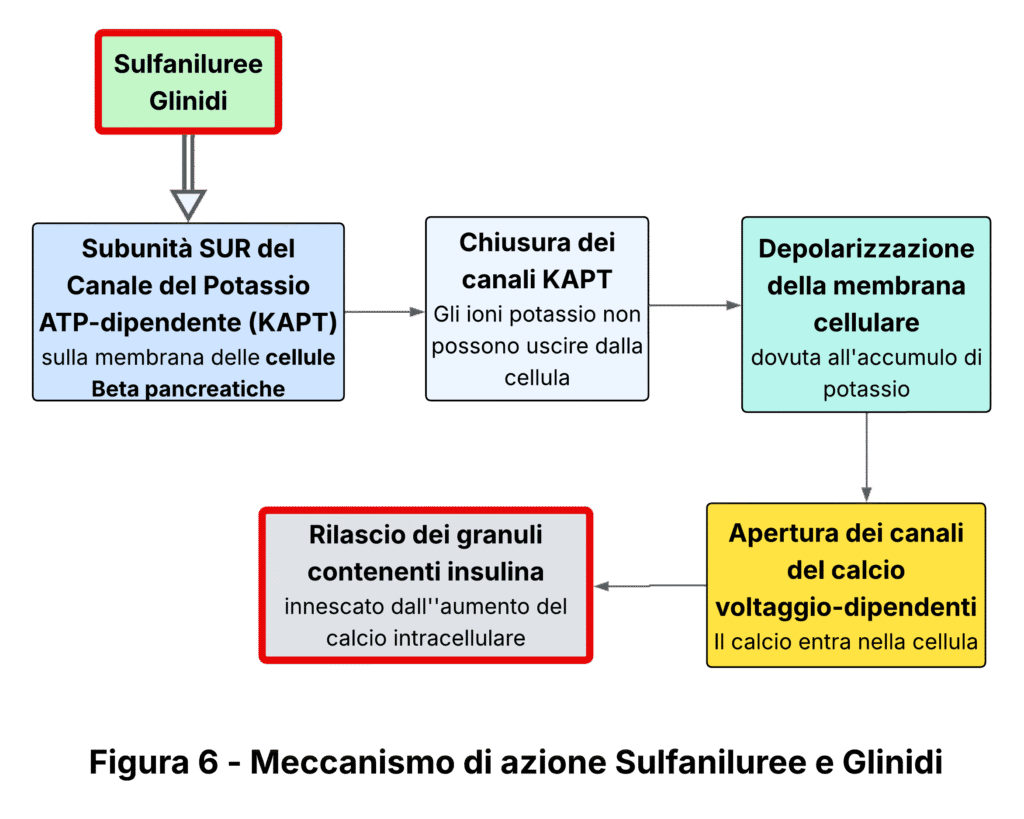
Questo legame determina la chiusura dei canali, bloccando efficacemente l’efflusso fisiologico degli ioni potassio verso l’ambiente extracellulare. In condizioni normali, questi canali mantengono la cellula in uno stato di riposo elettrico, ma la loro inibizione farmacologica altera drasticamente l’equilibrio ionico.
La conseguente ritenzione intracellulare di ioni potassio genera una progressiva depolarizzazione della membrana cellulare, modificando il gradiente elettrochimico transmembranario. Questo cambiamento del potenziale elettrico rappresenta il segnale scatenante per l’attivazione dei canali del calcio voltaggio-dipendenti di tipo L, presenti in alta densità sulla superficie delle cellule beta pancreatiche.
L’apertura di questi canali specializzati consente un massiccio afflusso di ioni calcio dall’ambiente extracellulare verso il citoplasma, determinando un rapido incremento della concentrazione intracellulare di questo importante secondo messaggero. L’aumento del calcio citoplasmatico innesca infine il processo di esocitosi, durante il quale i granuli secretori contenenti insulina pre-formata si fondono con la membrana plasmatica, liberando l’ormone nel circolo sanguigno attraverso un meccanismo calcio-dipendente altamente regolato.
La differenza principale tra sulfaniluree e glinidi sta nella cinetica d’azione:
- le sulfaniluree si legano più tenacemente al recettore, con effetto prolungato,
- mentre i glinidi hanno un’azione più rapida e breve.
Principali sulfaniluree
Le sulfaniluree si suddividono in due generazioni principali in base alla loro evoluzione farmacologica e alle caratteristiche cliniche.
La prima generazione comprende tolbutamide e clorpropamide, molecole ormai raramente utilizzate nella pratica clinica moderna a causa del loro profilo farmacologico meno favorevole e della maggiore incidenza di effetti collaterali.
La seconda generazione rappresenta l’evoluzione di questa classe farmacologica e include glibenclamide (nota anche come gliburide), glipizide, gliclazide e glimepiride. Questi composti presentano una maggiore potenza farmacologica, una durata d’azione più appropriata e un profilo di sicurezza migliorato rispetto ai predecessori, rendendoli più adatti all’impiego terapeutico contemporaneo nel trattamento del diabete tipo 2.
Principali glinidi
Le glinidi comprendono due principali rappresentanti farmacologici che differiscono per struttura chimica e caratteristiche farmacocinetiche.
La repaglinide, derivato dell’acido benzoico, rappresenta il capostipite di questa classe terapeutica e presenta un’emivita intermedia che consente una modulazione flessibile della secrezione insulinica in relazione ai pasti: è perciò adatta a pazienti con abitudini alimentari irregolari, e quando serve un controllo glicemico più prolungato postprandiale.
La nateglinide, derivato della D-fenilalanina, condivide il meccanismo d’azione con la repaglinide ma si distingue per una cinetica ancora più rapida, con un onset d’azione particolarmente veloce e una durata d’effetto più breve, caratteristiche che la rendono particolarmente adatta al controllo delle escursioni glicemiche postprandiali immediate. (es. pazienti con picchi glicemici precoci).
Inoltre crea minore accumulo in caso di pasti saltati (ridotto rischio ipoglicemia).
Efficacia clinica
- Riduzione dell’HbA1c (Emoglobina glicata): tipicamente 1-1,5%
- Rapida insorgenza d’azione: particolarmente per i glinidi, utile per il controllo dell’iperglicemia post-prandiale
Vantaggi
- Rapida efficacia: l’effetto ipoglicemizzante si manifesta velocemente, rendendo questi farmaci utili quando è necessaria una pronta riduzione della glicemia.
- Costo contenuto: soprattutto le sulfaniluree, essendo disponibili come generici, hanno un costo molto più basso rispetto ai farmaci innovativi.
- Comprovata esperienza clinica: decenni di utilizzo hanno fornito una solida esperienza sulla loro gestione.
Svantaggi ed effetti collaterali
- Ipoglicemia: il principale rischio, dovuto al fatto che stimolano la secrezione insulinica indipendentemente dai livelli glicemici. Il rischio è maggiore con:
- Sulfaniluree a lunga durata d’azione (glibenclamide)
- Pazienti anziani
- Insufficienza renale
- Salto dei pasti
- Esercizio fisico intenso
- Aumento di peso: in media 2-3 kg, dovuto sia all’effetto anabolico dell’aumentata insulinemia che alla necessità di frequenti spuntini per prevenire/trattare le ipoglicemie.
- Possibili effetti cardiovascolari: sebbene controverso, alcuni studi hanno suggerito un potenziale impatto negativo delle sulfaniluree sul rischio cardiovascolare, possibilmente legato alla loro capacità di interferire con il precondizionamento ischemico (un meccanismo protettivo cardiaco mediato dai canali KATP).
- Reazioni allergiche cutanee: relativamente rare, più frequenti con le sulfaniluree di prima generazione.
- Perdita di efficacia nel tempo (fallimento secondario): legato all’esaurimento progressivo delle cellule beta e alla ridotta capacità di risposta al farmaco.
Indicazioni cliniche
Oggi le sulfaniluree e i glinidi vengono utilizzati con maggiore cautela rispetto al passato, principalmente come:
- Terapia di seconda linea in pazienti con controllo glicemico insufficiente con la sola Metformina
- Opzione economica quando i costi rappresentano un fattore limitante
- Alternative in pazienti che non possono utilizzare altri farmaci per controindicazioni specifiche
L’utilizzo di questi farmaci è in calo a favore delle classi più moderne di antidiabetici, che offrono un miglior profilo di sicurezza e benefici aggiuntivi oltre al controllo glicemico.
Il Nostro Viaggio non Finisce Qui…
Con questo secondo appuntamento abbiamo completato l’analisi dei farmaci storicamente consolidati nella terapia del diabete mellito. Dalla terapia insulinica, protagonista assoluta del nostro primo articolo e pilastro insostituibile del trattamento del diabete tipo 1, siamo giunti a esplorare il trio farmacologico che ha rivoluzionato l’approccio al diabete tipo 2: la Metformina, con il suo meccanismo d’azione complesso e il profilo di sicurezza eccezionale, affiancata dalle Sulfaniluree e dalle Glinidi, secretagoghi insulinici che dialogano direttamente con le cellule Beta pancreatiche.
Questi farmaci hanno rappresentato per decenni lo standard terapeutico di riferimento, dimostrando efficacia clinica e sostenibilità economica. Tuttavia, la ricerca farmacologica non si è mai fermata, spinta dalla necessità di superare i limiti intrinseci di queste molecole e di rispondere alle esigenze di una popolazione diabetica sempre più complessa e diversificata.
Il nostro viaggio nella farmacologia antidiabetica si concluderà nel prossimo e ultimo capitolo, dove ci addentreremo nell’affascinante universo delle terapie innovative: dagli agonisti del GLP-1 agli inibitori SGLT-2, dalle molecole dual-action alle più recenti frontiere della medicina di precisione. Scopriremo come la rivoluzione terapeutica degli ultimi anni stia ridefinendo non solo il controllo glicemico, ma l’intera gestione cardiovascolare e renale del paziente diabetico.
Vi diamo appuntamento al terzo episodio per esplorare insieme il futuro della diabetologia.
Bibliografia
Chaudhary, S., & Kulkarni, A. (2024). Metformin: Past, Present, and Future. Current diabetes reports, 24(6), 119–130. https://doi.org/10.1007/s11892-024-01539-1
Petrie J. R. (2024). Metformin beyond type 2 diabetes: Emerging and potential new indications. Diabetes, obesity & metabolism, 26 Suppl 3, 31–41. https://doi.org/10.1111/dom.15756
Dihoum, A., Rena, G., Pearson, E. R., Lang, C. C., & Mordi, I. R. (2023). Metformin: evidence from preclinical and clinical studies for potential novel applications in cardiovascular disease. Expert opinion on investigational drugs, 32(4), 291–299. https://doi.org/10.1080/13543784.2023.2196010
Amer, B.E., Abdelgalil, M.S., Hamad, A.A. et al. Metformin plus lifestyle interventions versus lifestyle interventions alone for the delay or prevention of type 2 diabetes in individuals with prediabetes: a meta-analysis of randomized controlled trials. Diabetol Metab Syndr 16, 273 (2024). https://doi.org/10.1186/s13098-024-01504-8
Nabrdalik, K., Skonieczna-Żydecka, K., Irlik, K., Hendel, M., Kwiendacz, H., Łoniewski, I., Januszkiewicz, K., Gumprecht, J., & Lip, G. Y. H. (2022). Gastrointestinal adverse events of metformin treatment in patients with type 2 diabetes mellitus: A systematic review, meta-analysis and meta-regression of randomized controlled trials. Frontiers in endocrinology, 13, 975912. https://doi.org/10.3389/fendo.2022.975912
Wu, Z., Wang, W., Wei, L., & Zhu, S. (2023). Current status and frontier tracking of clinical trials on Metformin for cancer treatment. Journal of cancer research and clinical oncology, 149(18), 16931–16946. https://doi.org/10.1007/s00432-023-05391-w
Naseri, A., Sanaie, S., Hamzehzadeh, S., Seyedi-Sahebari, S., Hosseini, M. S., Gholipour-Khalili, E., Rezazadeh-Gavgani, E., Majidazar, R., Seraji, P., Daneshvar, S., & Rezazadeh-Gavgani, E. (2022). Metformin: new applications for an old drug. Journal of basic and clinical physiology and pharmacology, 34(2), 151–160. https://doi.org/10.1515/jbcpp-2022-0252
Lv, W., Wang, X., Xu, Q., & Lu, W. (2020). Mechanisms and Characteristics of Sulfonylureas and Glinides. Current topics in medicinal chemistry, 20(1), 37–56. https://doi.org/10.2174/1568026620666191224141617
Ashcroft F. M. (1996). Mechanisms of the glycaemic effects of sulfonylureas. Hormone and metabolic research = Hormon- und Stoffwechselforschung = Hormones et metabolisme, 28(9), 456–463. https://doi.org/10.1055/s-2007-979837
Pubblicità